Влияние ММСК и ГСК на репаративную регенерацию печени в условиях ее токсического повреждения
УДК 616.36-003.93:576.54
И.Ю. Маклакова 1, 2, В.В. Базарный 1, Д.Ю. Гребнев 1, 2
1 ФГБУ ВО «Уральский государственный медицинский университет», г. Екатеринбург, Российская Федерация;
2 ГАУЗ СО «Институт медицинских клеточных технологий», г. Екатеринбург, Российская Федерация
Резюме. Целью настоящего исследования стало изучение влияния сочетанной трансплантации ММСК и ГСК на показатели регенерации печени в условиях ее токсического повреждения тетрахлорметаном. Материалы и методы. Исследование выполнено на белых мышах-самцах с токсическим повреждением печени путем внутрибрюшинного введения тетрахлорметана в дозе 50 мкл на мышь однократно. Через час после моделирования повреждения печени осуществлялось внутривенное введение плацентарных ММСК и ГСК соответственно в дозе 4 млн. клеток/кг и 330 тыс. клеток/кг, суспендированные в 0,2 мл 0,9% раствора NaCl. Животным контрольной группы вводили 0,9% раствор NaCl — 0,2 мл внутривенно. На 1, 3, 7 сутки после трансплантации клеток производилась оценка изменения воспалительной активности в печени, определение митотического, апоптотического индексов. На 7 сутки после введения клеток производился анализ активности ферментов репарации ДНК семейства PARP. Результаты. Сочетанная трансплантация ММСК и ГСК приводит к снижению индекса воспалительной активности в печени вследствие уменьшения некроза, дистрофии гепатоцитов, снижения инфильтрации. В результате исследования установлено повышение активности ферментов репарации системы PARP, что привело к уменьшению запрограммированной клеточной гибели. Также котрансплантация ММСК и ГСК сопровождалась повышением митотической активности гепатоцитов. Заключение. Котрансплантация ММСК и ГСК в условиях токсического повреждения печени снижает воспалительную реакцию, стимулирует митотическую активность гепатоцитов, повышает активность ферментов системы репарации ДНК. Активация репаративной системы печени, в свою очередь, обеспечивает снижение запрограммированной гибели гепатоцитов.
Ключевые слова: мультипотентные мезенхимальные стромальные клетки, гемопоэтические стволовые клетки, токсический гепатит, репаративная регенерация печени
Конфликт интересов отсутствует.
Контактная информация автора, ответственного за переписку:
Гребнев Дмитрий Юрьевич
Дата поступления 03.12.2020 г.
Образец цитирования:
Маклакова И.Ю., Базарный В.В., Гребнев Д.Ю. Влияние ММСК и ГСК на репаративную регенерацию печени в условиях ее токсического повреждения. http://vestnikural.ru/article/1143. [Электронный ресурс] Вестник уральской медицинской академической науки. 2020, Том 17, №3, с. 243–248, DOI: 10.22138/2500-0918-2020-17-3-243-248
Введение
Печень — многофункциональный орган, участвующий в различных метаболических процессах, поэтому нарушение его функции приводит к серьезному нарушению обмена веществ в организме. Введение тетрахлорметана используется с 1928 года для изучения механизмов токсического повреждения печени на лабораторных животных [1]. Известно, что в повреждении печени важную роль играют активные формы кислорода. Тетрахлорметан в клетках печени метаболизируется под влиянием цитохрома P-450 с образованием активных форм кислорода [2]. Окислительный стресс, вызванный большим количеством свободных радикалов, вызывает повреждение печени. В настоящее время продолжается поиск эффективных способов восстановления структуры и функции печени после ее токсического повреждения. Перспективным в лечении повреждений печени представляется использование котрансплантации двух видов клеток: мультипотентных мезенхимальных стромальных (ММСК) и гемопоэтических стволовых клеток (ГСК). ММСК способны к синтезу противовоспалительных цитокинов, факторов роста [3, 4]. Иммуномодулирующие свойства ММСК позволяют проводить сочетанную трансплантацию двух видов клеток [5]. Доказана способность ГСК активировать регенерацию печени как путем дифференцировки в гепатоциты, так и с помощью слияния с клетками печени (fusion-effect). Кроме того, ММСК секретируют SDF-1 (Stromalderivedfactor-1), который стимулирует миграцию аллогенных и аутологичных ГСК в поврежденную печень [6]. Перспективным источником стволовых клеток является плацента, так как получение ее не связано с оперативным вмешательством и не влечет за собой этических проблем. Кроме того, плацентарные клетки обладают большим пролиферативным и дифференцировочным потенциалом. Таким образом, целью данного исследования стало изучение влияния котрансплантации плацентарных ММСК и ГСК на репаративную регенерацию печени в условиях ее токсического повреждения.
Материалы и методы
Эксперименты выполнены на 42 белых мышах-самцах возраста 7-8 месяцев, массой 20-23 г. Производилось выделение культуры ММСК из хориона плаценты 5 лабораторных животных мышей-самок возраста 3-4 месяца, срок гестации 18 дней. Мононуклеарная фракция клеток была получена путем последовательной механической и ферментативной (раствор аккутазы (Millipore, США)) обработки ткани плаценты. Выделение ГСК осуществлялось методом позитивной иммуномагнитной сепарации по антигенам SCA-1 (StemCell Technologies, СШA) и CD 117 (StemCell Technologies, СШA) (X. Muniraetal., 2009).Все эксперименты, уход и содержание животных осуществлялись в соответствии с Директивой №63 от 22 сентября 2010 года Президиума и Парламента Европы «О защите животных, используемых для научных исследований» и приказом Минздрава РФ № 267 от 19.06.2003 «Об утверждении правил лабораторной практики». Выполнение исследований одобрено локальным этическим комитетом ФГБОУ ВО «Уральский государственный медицинский университет» протокол №8 от 20.10.2017.
Культивирование ММСК проводилось в условиях СО2 — инкубатора (TermoScientific, США) при температуре 37 °C с содержанием углекислого газа 5% и влажностью 90%. Для трансплантации лабораторным животным были использованы ММСК третьего пассажа. Идентификация ММСК проводилась иммуноцитохимическим методом с использованием набора MesenchymalStemCellCharacterizationKit (Millipore, США), содержащего позитивные (антитела к integrin β1, CD 54, collagentypeI и fibronectin) и негативные маркеры (антитела к CD 14, CD 45). Изучение функциональных свойств выделенных клеток было проведено путем направленной дифференцировки полученной культуры в направлениях, характерных для ММСК — в адипоцитарном и остеогенном. Идентификация ГСК была проведена на проточном цитометре BeckmanCoulterNavios. В суспензии трансплантируемых клеток оценивалось содержание ГСК с иммунофенотипом положительных по CD117, Sca-1 и отрицательных по Lin- (CD45, С3е, Ly-6G, M1/70, Ter-119). Содержание клеток после иммуномагнитной сепарации с иммунофенотипом CD117+, Sca-1+, Lin- составило 80-93%. Жизнеспособность клеток была определена с помощью суправитальной окраски раствором трипанового синего и перед трансплантацией составила 95-97%. Животным опытной группы внутривенно вводились ММСК и ГСК соответственно в дозе 4 млн клеток/кг и 330 тыс. клеток/кг, суспендированные в 0,2 мл 0,9% раствора NaCl. Животным контрольной группы вводили 0,9% раствор NaCl — 0,2 мл внутривенно. Внутривенные введения осуществлялись через 1 час после введения тетрахлорметана.
Исследовалось влияние сочетанной трансплантации ММСК и ГСК на показатели регенерации печени на 1, 3, 7 сутки после внутрибрюшинного введения тетрахлорметана в дозе 50 мкл на мышь однократно.Из опыта животных выводили декапитацией под легким эфирным наркозом. Изготавливали гистологические срезы печени толщиной 3-5 мкм, окрашивали гематоксилином-эозином. Для морфометрического анализа данных использовали компьютерную программу анализа изображений (Biovision, Россия). С этой целью производили микрофотосъемку случайных полей зрения гистологических препаратов цифровой камерой OLYMPUS XC30 на базе микроскопа OLYMPUS BX51 (OLYMPUS, Япония) при увеличении ×100, ×200, ×400, ×600, ×1000 (не менее 10 полей зрения в каждом гистологическом срезе).
Для количественной оценки выраженности воспалительных явлений в ткани печени был введен индекс воспалительной активности (ИВА). При этом производился анализ следующих гистологических изменений: 1) некрозы гепатоцитов – оценивались от 0 до 10 баллов; 2)дистрофия гепатоцитов % оценивались от 0 до 4 баллов; 3) воспалительный инфильтрат % оценивался от 0 до 4 баллов. ИВА определялся по сумме полученных баллов. Также производился расчет митотического индекса (МИ) гепатоцитов, апоптотического индекса (АИ), выраженные в промилле. Верификация выраженности апоптоза осуществлялась с использованием метода ApopTag® PeroxidaseInSituOligoLigation (ISOL) (Millipore, США).Апоптотический индекс определялся как отношение числа клеток в состоянии апоптоза к общему числу подсчитанных гепатоцитов.
С целью оценки выраженности репаративных процессов в клетках печени производился анализ количества Поли-АДФ-рибозаполимера (PARP), который является продуктом реакции Поли-АДФ-рибозилирования. По количеству этого полимера можно судить об активности ферментов репарации ДНК. Определение уровня данного показателя осуществлялось в клетках печени с использованием первичных (Anti-Poly (ADP-Ribose) Polymer antibody, abcam) и вторичных антител (Rabbit Anti-Chicken IgY H&L (FITC), abcam) на проточном цитометре Beckman Coulter по методу A. Kunzmann, D. Lui, K. Annett на 7 сутки после моделирования токсического повреждения печени. Определялась средняя интенсивность флуоресценции популяции клеток (MFI), которая служит количественным критерием, характеризующим экспрессию антигенов (плотность рецепторов) внутри клетки.
Достоверность отличий в сравниваемых выборках проведено с применением t-критерия Стьюдента. Статистическая обработка данных проведена с помощью программного пакета SPSSStatistics (версия 17,0).
Результаты и обсуждения
Повреждение печени тетрахлорметаном сопровождается развитием воспалительной реакции с гиперпродукцией цитокинов и хемокинов. На гистологических препаратах печени наблюдаются зоны некрозов, вакуольная дистрофия гепатоцитов, лимфоцитарная инфильтрация. На первые сутки после сочетанного введения ММСК и ГСК на фоне токсического повреждения печени при анализе выраженности индекса воспалительной активности в печени не выявлено достоверных отличий между опытной и контрольной группами. На 3 сутки после введения тетрахлорметана в опытной группе получено уменьшение инфильтрации и дистрофии гепатоцитов, что привело к снижению индекса воспалительной активности. На 7 сутки также имеются отличия между опытной и контрольной группами. Снижение индекса воспалительной активности произошло за счет сокращения зон некрозов, уменьшения дистрофии гепатоцитов, снижения воспалительной инфильтрации (таблица 1). Уменьшение интенсивности воспалительного процесса в печени может быть обусловлено способностью ММСК к синтезу спектра противовоспалительных цитокинов (TGF-β, ИЛ-10), а также ГСК к синтезу TGF-β. Известно, что TGF-β оказывает противовоспалительное действие за счет уменьшения выработки клетками иммунной системы ИЛ-1, ФНО, за счет торможения пролиферации Т- и В-лимфоцитов, подавления активности макрофагов.
Таблица 1
Выраженность воспалительных явлений в печени мышей после введения CCl4, M±m, n=7
Показатели | 1 сутки | 3 сутки | 7 сутки | |||
NaCl | ММСК+ГСК | NaCl | ММСК+ГСК | NaCl | ММСК+ГСК | |
Некрозы, баллы | 6,0±0,52 | 5,1±0,49 | 5,6±0,50 | 4,7±0,42 | 3,8±0,32 | 3,1±0,28* |
Дистрофия гепатоцитов, баллы | 3,1±0,24 | 2,8±0,20 | 2,9±0,22 | 2,4±0,20* | 2,0±0,17 | 1,6±0,12* |
Воспалительный инфильтрат, баллы | 3,3±0,30 | 2,9±0,25 | 3,1±0,21 | 2,5±0,18* | 2,2±0,23 | 1,7±0,14* |
Итого ИВА: | 12,4±1,13 | 10,8±0,93 | 11,6±1,08 | 9,6±0,88* | 8,0±0,81 | 6,4±0,57* |
Примечание: * отличие от контрольной группы животных, достоверно с p<0,05
Введение тетрахлорметана привело к повышению митотической активности гепатоцитов. Это произошло в результате выраженного воспалительного ответа в печени, что сопровождается повышенной экспрессией транскрипционного фактора NF-kB, который усиливает пролиферацию гепатоцитов [7]. Развивающая в очаге воспаления гипоксия, накопление активных форм кислорода повреждают мембрану митохондрий, что ведет к высвобождению цитохрома С. В результате активируется каспаза 9 и запускается процесс апоптоза.
Токсическое повреждение печени вызывает компенсаторное повышение активности ферментов репарации ДНК семейства PARP. После котрансплантации ММСК и ГСК установлено еще большее повышение активности этих ферментов по сравнению с контрольной группой (рисунок 1).
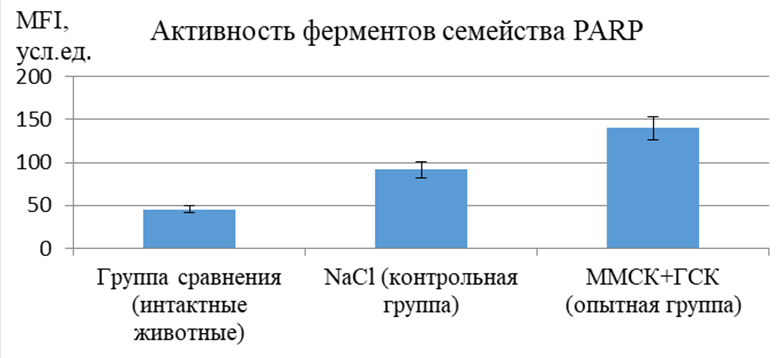
Рис.1. Показатели активности ферментов репарации ДНК семейства PARP
Возможным механизмом активации системы репарации ДНК может быть способность трансплантируемых ММСК индуцировать в клетках синтез белков теплового шока (70 кД) — шаперонов [8, 9]. Эти белки обеспечивают поддержание структуры и функции ферментов репарации в условиях действия повреждающего фактора. Повышение уровня ферментов системы репарации ДНК приводит к уменьшению количества повреждений в клетке, что снижает активацию инициирующих и эффекторных каспаз и, как следствие, угнетает выраженность запрограммированной клеточной гибели.
В результате исследования получено, что котрансплантация ММСК и ГСК уже на 1 сутки после моделирования токсического повреждения печени приводит к активации митотической активности гепатоцитов, а на 3 сутки – к снижению запрограммированной клеточной гибели (таблица 2). Повышение митотического индекса в опытной группе можно объяснить способностью ММСК к синтезу фактора роста гепатоцитов — HGF. Известно, что HGF является митогеном для гепатоцитов, а также способствует дифференцировке перисинусоидальных клеток печени в гепатоциты. Также повышению митотической активности гепатоцитов может способствовать fusion-effect –способность ГСК к слиянию с гепатоцитами.
Таблица 2
Показатели регенераторной активности гепатоцитов после введения CCl4, M±m, n=7
| Группы животных | Показатели | |
МИ, ‰ | АИ, ‰ | ||
Интактные животные | 0,48±0,07 | 0,41±0,05 | |
1 сутки | NaCl (контрольная группа) | 17,74±2,13* | 4,87±0,36* |
ММСК+ГСК (опытная группа) | 22,04±1,53* ** | 4,34±0,36* | |
3 сутки | NaCl (контрольная группа) | 15,20±1,20* | 3,70±0,31* |
ММСК+ГСК (опытная группа) | 20,40±1,60* ** | 2,67±0,23* ** | |
7 сутки | NaCl (контрольная группа) | 17,06±1,64* | 3,74±0,31* |
ММСК+ГСК (опытная группа) | 23,56±1,85* ** | 2,67±0,20* ** | |
Примечание: * отличие от группы интактных животных, достоверно с p<0,05; ** отличие от контрольной группы животных, достоверно с p<0,05;
Выводы
Полученные результаты свидетельствуют о способности сочетанной трансплантации ММСК и ГСК снижать выраженность воспалительной реакции в печени при ее токсическом повреждении. Также котрансплантация ММСК и ГСК стимулирует митотическую активность гепатоцитов, повышает активность ферментов системы репарации ДНК. Активация репаративной системы печени, в свою очередь, обеспечивает снижение запрограммированной гибели гепатоцитов.
ЛИТЕРАТУРА
1. Minot A.S, Cutler J.T. Guanidine retention and calcium reserve as antagonistic factors in carbon tetrachloride and chloroform poisoning / A.S. Minor, J.T. Cutler // J Clin Invest. – 1928. — 6(3): 369.
2. Guo, Q. Liver metabolomics study reveals protective function of Phyllanthus urinaria against CCl4-induced liver injury / Q. Guo // Chinese journal of natural medicines. — 2017. — 15 (7). — 525–0533.
3. Hu C. Chenxia Hu, Lanjuan Li. Preconditioning influences mesenchymal stem cell properties in vitro and in vivo // Journal of Cellular and Molecular Medicine. – 2018. – Vol. 22(3). – P. 1428-1442.
4. Alfaif M. Mesenchymal stromal cell therapy for liver diseases / Mohammed Alfaifi, Young Woo Eom, Philip N. Newsome [et al.] // Journal of Hepatology. – 2018. – Vol.68. – P. 1272-1285.
5. S. F. H. de Witte, Franquesa M., Baan C. C., Hoogduijn M. J. “Toward development of iMesenchymal stem cells for immunomodulatory therapy,” Frontiers in Immunology. – 2016. — Vol. 6. — P. 648.
6. Brown Ch. Mesenchymal Stem Cells: Cell Therapy and Regeneration Potential / Ch. Brown, Ch. McKee, Sh. Bakshi[et al.] // Journal of Tissue Engineering and Regenerative Medicine. – 2019. — Vol. 13(9). – P. 1738-1755.
7. Konishi T. “Hepatic ischemia/reperfusion: mechanisms of tissue injury, repair, and regeneration,” / T. Konishi, A. B. Lentsch // Gene Expression. – 2017. — Vol. 17. — №. 4. — P. 277–287.
8. Fitter S., Gronthos S., Ooi S.S., Zannettino A.C.W. “The mesenchymal precursor cell marker antibody STRO-1 binds to cell surface heat shock cognate 70,” Stem Cells. – 2017. — Vol. 35. №. 4. — P. 940–951.
9. Human umbilical cord mesenchymal stem cells protect against SCA3 by modulating the level of 70 kD heat shock protrin / T. Li, Y. Liu, L Yu [et al.] // Cellular and molecular neurobiolody. – 2018. – Vol 38. – P. 641–655.
Авторы
Маклакова Ирина Юрьевна
ФГБОУ ВО Уральский государственный медицинский университет Минздрава России
Кандидат медицинских наук, доцент кафедры патологической физиологии
Российская Федерация, 620028 г. Екатеринбург, ул. Репина 3
ГАУЗ СО «Институт медицинских клеточных технологий»
Старший научный сотрудник
Российская Федерация, 620026 г. Екатеринбург, ул. Карла Маркса 22а
Базарный Владимир Викторович
ФГБОУ ВО Уральский государственный медицинский университет Минздрава России
Доктор медицинских наук, профессор кафедры клинической лабораторной диагностики и бактериологии
Российская Федерация, 620028 г. Екатеринбург, ул. Репина 3
Гребнев Дмитрий Юрьевич
ФГБОУ ВО Уральский государственный медицинский университет Минздрава России
Доктор медицинских наук, заведующий кафедрой патологической физиологии
Российская Федерация, 620028 г. Екатеринбург, ул. Репина 3
ГАУЗ СО «Институт медицинских клеточных технологий»
Старший научный сотрудник
Екатеринбург, 620026 г. Екатеринбург, ул. Карла Маркса 22 а

