Особенности получения первичной культуры карциномы молочной железы
УДК:616-006.699
А.С. Могиленских 1, 2, С.В. Сазонов 1, 2, Д.В. Седнева-Луговец 1, С.М. Демидов 1, 2
1 ГАУЗ СО «Институт медицинских клеточных технологий», г. Екатеринбург, Российская Федерация;
2 ФГБОУ ВО Уральский государственный медицинский университет, г. Екатеринбург, Российская Федерация
Резюме. Материалы и методы. Полученные в ходе операции образцы подвергались диссоциации и помещались в различные условия для культивирования в 48-луночные планшеты. После 7 дней клетки фиксировали и окрашивали флуоресцентным красителем DAPI, подсчет клеток производился в программе ImageG. Результаты. При морфологической оценке клеток было выделено две группы прикрепленных клеток: близко расположенные друг к другу клетки треугольной формы, ядра плотно прилежат друг к другу — эпителиоподобный фенотип и клетки с многочисленными отростками, ядра расположены далеко друг от друга — фибробластоподобный фенотип. В ходе эксперимента производился контроль на 1е, 5е и 7е сутки. В среде Epicult™, также как и в среде Mammocult™ видно увеличение количества клеток и формирование клетками «маммосфер» при исследовании 1 осадка, покрытие коллагеном. Заключение. Проблемы при культивировании двухмерной клеточной культуры можно решить использованием подложки — коллагена, а также использованием обогащенной среды или коммерческой среды.
Ключевые слова: первичная культура, карцинома молочной железы
Конфликт интересов отсутствует.
Контактная информация автора, ответственного за переписку:
Могиленских Анна Сергеевна
annasajler@yandex.ru
Дата поступления 26.11.2020 г.
Образец цитирования:
Могиленских А.С., Сазонов С.В., Седнева-Луговец Д.В., Демидов С.М. Особенности получения первичной культуры карциномы молочной железы. http://vestnikural.ru/article/1144. [Электронный ресурс] Вестник уральской медицинской академической науки. 2020, Том 17, №3, с. 249–256, DOI: 10.22138/2500-0918-2020-17-3-249-256
Введение
При получении первичной культуры клеток человека часто возникают проблемы при выделении клеток из хирургического материала (низкое качество материала, шок клеток при переходе из одной среды в другую), при поддержании клеточной культуры в стабильном состоянии (раннее старение), при получении нужной популяции клеток.
Первой проблемой при первичном культивировании карциномы молочной железы (КМЖ) был чрезмерный рост фибробластов, которые быстро приспосабливаются к условиям in vitro и размножаются быстрее, чем эпителиальные клетки [1]. Более 20 лет назад McCallum H. M. и Lowther G. W (1996) разработали методику, при которой образец опухоли разрезали на тонкие пласты и собирали клетки, выделяющиеся в питательную среду. При использовании методики авторы смогли выделить 10 клеточных линий из 135 опухолей молочной железы [2, 3].
Нуштаева А.А. (2019) в своей работе описала метод, при котором клетки получали из транспортировочной среды, объединенной с раствором после промывания и измельчения образцов ткани. Данные клетки, полученные без использования коллагеназы, проявляли большую адегезивную способность (36 часов в среднем, в отличие от ферментативно полученных клеток — 72 часа в среднем) и имели эпителиоподобный фенотип клеток среди фибробластоподобных [4].
Вторая проблема, которая возникает в ходе культивирования, это поддержание эпителиальной природы клеток в ходе нескольких пассажей и подбор соответствующей питательной среды. Наиболее популярным решением является среда, дополеннная ингибитором Rho-киназы (ROCK) [5].
В 2016 году Janik К. и соавт. сравнивали рост культуры клеток рака молочной железы в коммерческой среде EpiCult и тканеспецифичной среде ВСMP (DMEM: F12, дополненная человеческой сывороткой (2%; Sigma-Aldrich), пенициллин/стрептомицин (1%), гентамицин (0,2%), EGF (10 нг/мл), аденин (20 мкг/мл), CHTX (8,4 нг/мл), HEPES (15 мМ ), инсулин (5 мкг/мл), гидрокортизон (0,32 мкг/мл) и ингибитор ROCK (10 мкМ)). Было показано [6], что в коммерческой среде наблюдается меньший рост клеток, даже при условии добавления ингибитора ROCK (рис. 1).
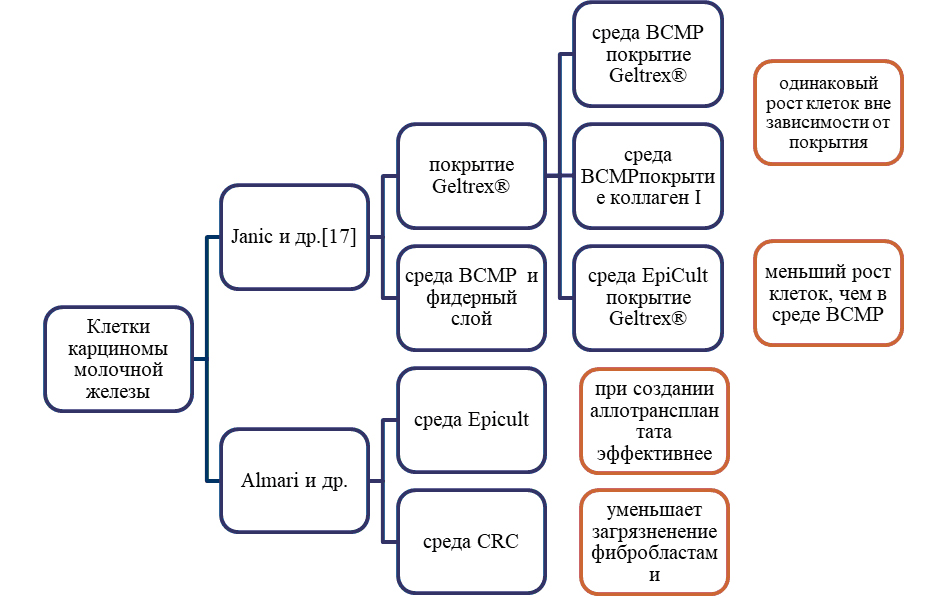
Рис 1. Схема экспериментального рабочего процесса — различные попытки культивировать первичные эпителиальные клетки молочной железы.
Almari А.М. и др. (2016) также сравнивали действие на рост культуры клеток рака молочной железы двух сред — EpiCult и CRC (F, содержащей 25% питательной смеси Ham-F-12 с добавлением 25 нг/мл гидрокортизона, 5 мкг/мл инсулина, 0,1 нмоль/л холерного токсина, 0,125 нг/мл эпидермального фактора роста, 10 мкг/мл гентамицина, 250 нг/мл) и 5 мкмоль/л ингибитора ROCK Y-27632). Было обнаружено, что использование CRC не только увеличивало количество полученных культур, но также уменьшало загрязнение их фибробластами (рис. 2). Однако, при создании аллотрансплантанта более быстрое развитие было показано с EpiC-культивируемыми клетками. Хотя использование CRC способствует сохранению архитектуры эпителиальных клеток, но не приводит к лучшему сохранению транскриптома рака в процессе культивирования [7].
Среды, с которыми проводились исследования, содержали помимо ингибитора ROCK, гидрокортизон и холерный токсин.
Esparza-López J. и соавт. (2016) в своей работе не использовали в среде для роста первичной культуры холерный токсин, рост клеточной линии осуществлялся на основе среды RPMI 1640 с добавлением 2,0 мМ глютамина, 0,005 мг/мл инсулина, 5,0 нг/мл EGF, 0,5 мкг/мл гидрокортизона, 5,0 мкг/мл трансферрина, 0,1 мкМ изопротеренола, 0,01 мкМ этаноламина и 0,01 мкМ о-фосфоэтаноламина [8].
Помимо этих сред, используются также готовые коммерческие среды, такие как Mammocult™ [9-12].
Третьей проблемой, существующей при культивировании клеток КМЖ, является плохая адгезивность к поверхности эпителиальных клеток. Это привело к разработке различных стратегий, в которых используются не только специальные обогащенные среды, но и питающий слой [13, 14]. Для поддержки роста эпителиальных клеток в культуре необходимо создание подложки, на которой эти клетки смогут поддерживать стабильный рост популяции. Часто используется фидерный слой — живые клетки, например, фибробласты, которые выделяют необходимые факторы роста для эпителиальной культуры. Таким способом было получено несколько первичных опухолей с доказанной эпителиальной природой [15, 16].
Однако, используемые в качестве такого слоя клетки также могут трансформироваться и подвергаться старению, а подготовка такого слоя занимает длительное время. Более того, не всегда есть техническая возможность подготовить данное покрытие. Могут быть использованы и другие варианты – применение покрытия поверхности коллагеном или коммерческие покрытия [6].
Эксперимент, проведенный Janik К. и др., (2016) показал (рис 1.), что первичные клетки рака молочной железы одинаково эффективно размножаются на фидерном слое и на коммерческом покрытии Geltrex®, однако, после второго пассажа все меньше клеток прикрепляется к фидерному слою. При замене покрытием Geltrex® на коллаген I — существенных изменений не было обнаружено, что позволяет использовать покрытие коллагеном взамен дорогостоящего покрытия Geltrex® [6].
В данной работе был проведен эксперимент по сравнению культивирования клеток на коммерческих обогащенных питательных средах — Epicult и Mammocult при использовании различных осадков и покрытий — адгезивного, коллагена и неадгезивного покрытия. Среда Mammocult™ это бессывороточная культуральная среда, оптимизированная для культивирования маммосфер из нормальных первичных тканей молочной железы человека, Epicult™ также бессывороточная среда, но оптимизированная для получения монослоя эпителиальных клеток.
Материалы и методы исследования
В ходе операций было получено два биоптата карциномы молочной железы справа.
Полученные образцы в течение двух — трех часов транспортировали в лабораторию в стерильных условиях, измельчались до однородной массы и помещались в среду для диссоциации (4 мг/мл коллагеназы, 1 мг/мл гиалуронидазы, 0,1% трипсина, DMEM:F-12). После инкубирования около 20 часов при 37°C в отсутствии CO2 полученная масса делилась на осадки. Для получения первого осадка пробирку центрифугировали при 0,7 RPM и получали осадок 1(1 ос.), предположительно, обогащенный эпителиальными клетками. Супернатант центрифугировали 3 минуты 0,2 RPM, затем снова переносили супернатант и центрифугировали 5 минут при 1,4 RPM. Полученные осадки смешивали, ресуспендировали с трипсином и с раствором Хэнкса с 2% FBS(HF), центрифугировали 5 минут при тех же оборотах получали осадок 2. 1 осадок и 2 осадок растворяли в диспазе и ДНКе в течение 1-2 минут до получения тягучей массы, смешивали с HF и центрифугировали при 1,4 RPM. Далее оба осадка разводили с полной средой Mammocult и и 5% FBS и Epicult c 5%FBS, клетки высаживали в 48-луночные планшеты адгезивные, часть из которых была предварительно покрыта коллагеном (1:45) и на неадгезивные планшеты. На второй день не прикрепившиеся клетки собирали и центрифугировали, меняли среду на бессывороточную. После 7 дней клетки фиксировали и окрашивали флуоресцентным красителем DAPI, подсчет клеток производился в программе ImageG. Статистическая обработка производилась в программе MS Exel.
Результаты и их обсуждение
В ходе эксперимента производился контроль на 1е, 5е и 7е сутки. В среде Epicult™, также как и в среде Mammocult™ видно увеличение количества клеток и формирование клетками «маммосфер» при исследовании 1 осадка, покрытие коллагеном (рис. 2).
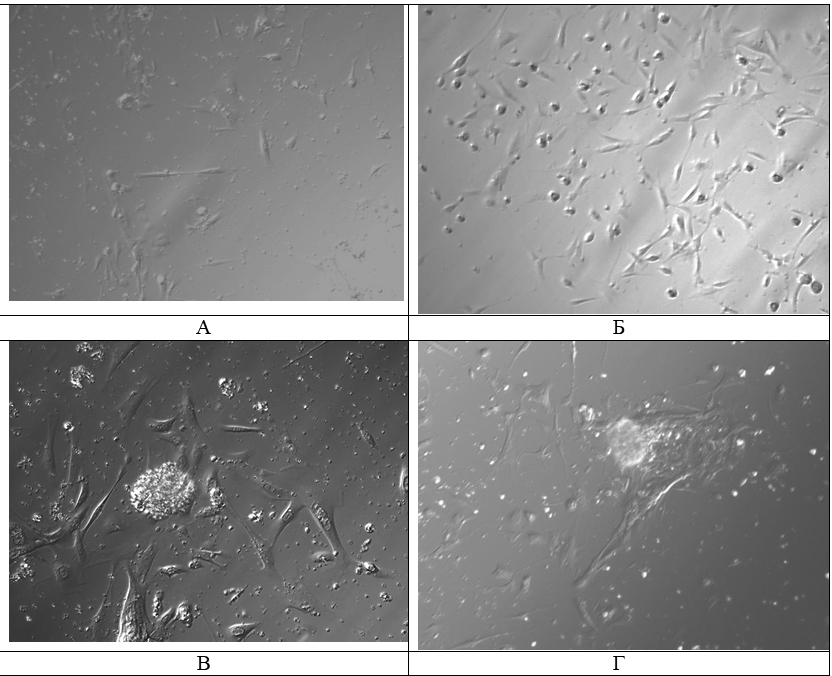
Рисунок 2. Рост клеток первичной культуры на 5е сутки (А) и (В) — среда Epicult™ и Mammocult™, и на 7е сутки (Б) и (Г) среда Epicult™ и Mammocult™, покрытие коллаген, 1 осадок, ув. ×100
При подсчете клеток в двух экспериментах наибольшее количество наблюдалось на среде Epicult™ при покрытии коллагеном и на адгезивном флаконе. При культивировании в среде Mammocult™ рост клеток на обоих покрытиях был меньше. Однако, при статистической оценке между данными покрытиями существенных различих обнаружено не было. В целом меньшее количество клеток наблюдалось во втором осадке на всех покрытиях (рис. 3).
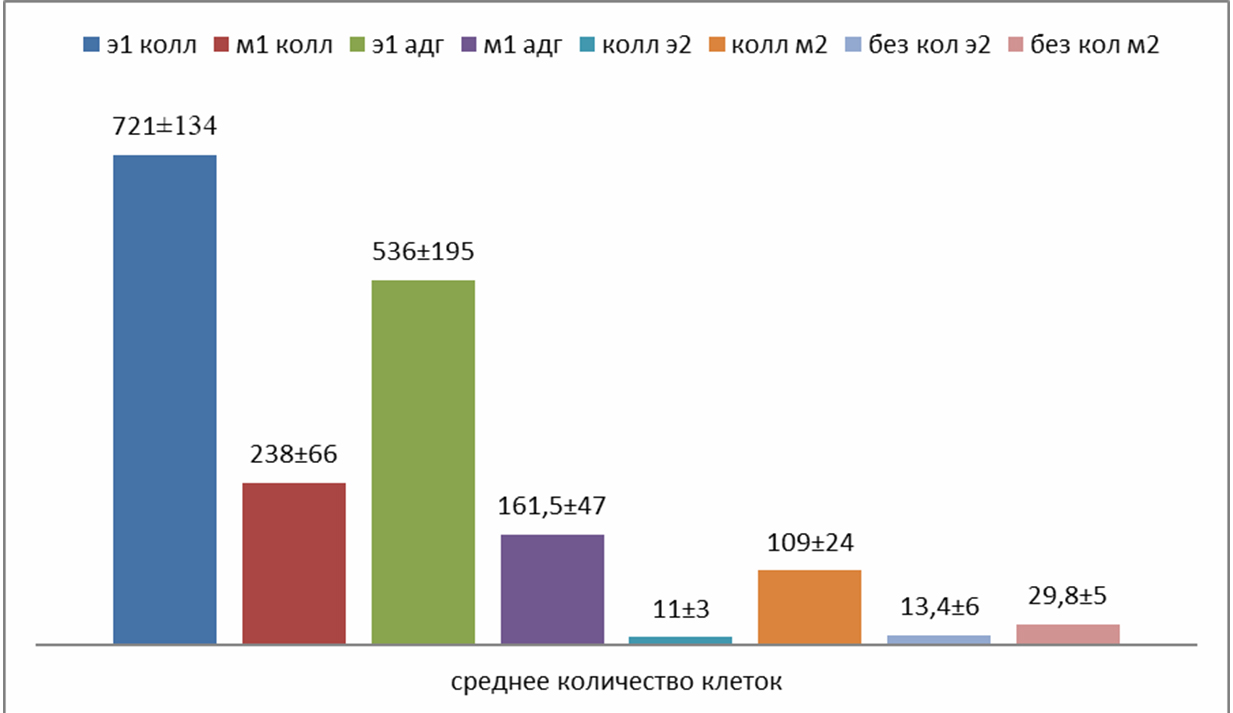
Рисунок 3. Среднее количество клеток в двух экспериментах.
При морфологической оценке клеток было выделено две группы прикрепленных клеток: близко расположенные друг к другу клетки треугольной формы, ядра плотно прилежат друг к другу — эпителиоподобный фенотип и клетки с многочисленными отростками, ядра расположены далеко друг от друга — фибробластоподобный фенотип. (рис. 4)
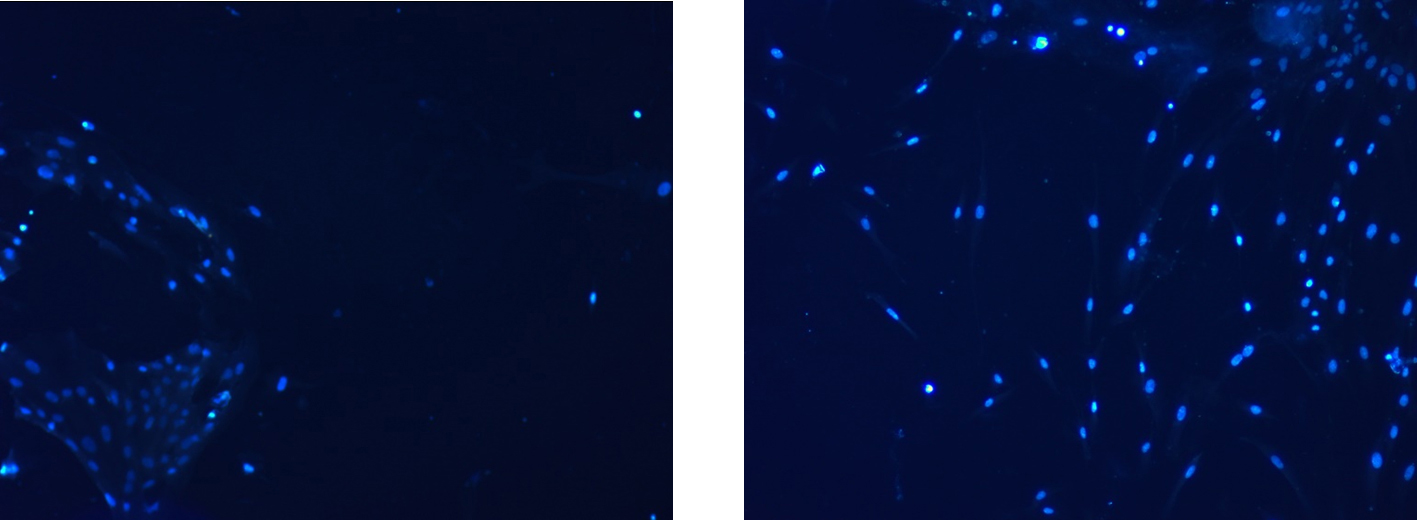
Рисунок 4. Морфология клеток в первичной культуре карциномы молочной железы. Окраска Dapi, ув. ×100
Заключение
Общая схема эксперимента представлена на рис. 5. Больший рост клеток был обнаружен в лунках с покрытием коллагеном на двух коммерческих средах.
При сравнении покрытия коллагеном и использования адгезивного флакона без покрытия было показано, что использование коллагена способствует ускорению роста и прикрепления клеток. В то время использование разных коммерческих сред, таких как Epicult и Mammocult, существенной разницы при культивировании не дает и использование любой из этих сред приводит к положительному результату [17, 18] .
Таким образом, проблемы при культивировании двухмерной клеточной культуры можно решить использованием подложки-коллагена, а также использованием обогащенной среды или коммерческой среды.
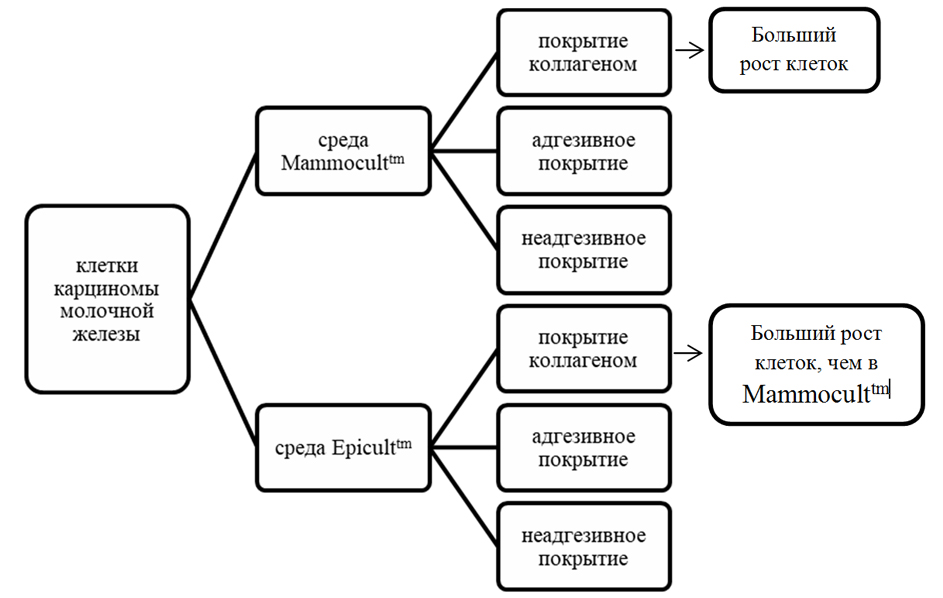
Рисунок 5. Схема эксперимента
ЛИТЕРАТУРА
1. Freshney R.I.: Induction of differentiation in neoplastic cells. Anticancer Res. 1985, 5: 111-130.
2. McCallum, H.M., Lowther, G.W. (1996). Long-term culture of primary breast cancer in defined medium. Breast Cancer Research and Treatment, 39(3), 247–259.
3. Mitra A., Mishra L., Li S. Technologies for deriving primary tumor cells for use in personalized cancer therapy. Trends Biotechnol. 2013;31(6):347-354.
4. Нуштаева А.А. Культуры онкотрансформированных клеток молочной железы и эндометрия для изучения опухолевой прогрессии и разработки терапевтических подходов [диссертация]. Новосибирск: Институт химической биологии и фундаментальной медицины СО РАН; 2019
5. Liu, Xuefeng et al. ROCK Inhibitor and Feeder Cells Induce the Conditional Reprogramming of Epithelial Cells The American Journal of Pathology, Volume 180, Issue 2, 599-607.
6. Janik K., Popeda M., Peciak J., et al. Efficient and simple approach to in vitro culture of primary epithelial cancer cells. Biosci Rep. 2016. Vo. 36(6).
7. Alamri A.M., Kang K., Groeneveld S., et al. Primary cancer cell culture: mammary-optimized vs conditional reprogramming. Endocr Relat Cancer. 2016;23 (7): 535–554.
8. Esparza-López J., Ramos-Elías P.A., Castro-Sánchez A. et al. Primary breast cancer cell culture yields intra-tumor heterogeneous subpopulations expressing exclusive patterns of receptor tyrosine kinases. BMC Cancer 16, 740 (2016).
9. Сазонов С.В., Бриллиант А.А., Фадеев Ф.А., Демидов С.М., Леонтьев С.Л. Опыт культивирования клеток карциномы молочной железы люминального подтипа. Вестник уральской медицинской академической науки. 2018, Том 15, №6, с.860-867
10. Сазонов С.В., Бриллиант А.А., Фадеев Ф.А., Улитко М.В., Денисенко С.А., Демидов С.М Изменение рецепторов клеток карциномы молочной железы люминального В подтипа при культивировании. Морфология, 2019. Т.155, №2, YIII Съезд научного медицинского общества анатомов, гистологов и эмбриологов, 23-26 мая, г. Воронеж, С. 248.
11. Шамшурина Е.О., Могиленских А.С., Сазонов С.В., Улитко М.В., Демидов. С.М. Опыт культивирования клеток карциномы молочной железы тройного негативного подтипа. Материалы VIII межрегиональной научно-практической конференции: Клеточные технологии – практическому здравоохранению, 3-4 декабря, 2019, г. Екатеринбург, С. 212-214.
12. Шамшурина Е.О., Могиленских А.С., Сазонов С.В., Улитко М.В., Демидов С.М., Титова С.А. Морфологический анализ культуры клеток рака молочной железы. Успехи молекулярной онкологии, 2019, Т.6., №4, С. 88-89. Материалы V Всероссийской конференции по молекулярной онкологии, 16-18 декабря 2019 г., Москва
13. Cobleigh M.A., Kennedy J.L., Wong A.C., Hill J.H., Lindholm K.M., Tiesenga J.E., Kiang R., Applebaum E.L., McGuire W.P. Primary culture of squamous head and neck cancer with and without 3T3 fibroblasts and effect of clinical tumor characteristics on growth in vitro, Cancer, 1987, 59.1732-1738.
14. Wang C.S., Goulet F., Tremblay N., Germain L., Auger F., Têtu B. Selective culture of epithelial cells from primary breast carcinomas using irradiated 3T3 cells as feeder layer, Pathol. Res. Pract., 2001, 197. 175-181.
15. Krasna L., Dudorkinova D., Vedralova J., Vesely P., Pokorna E., Kudlackova I., Chaloupkova A., Petruzelka L., Danes J., Matouskova E.: Large expansion of morphologically heterogeneous mammary epithelial cells, including the luminal phenotype, from human breast tumours. Breast Cancer Res Treat. 2002, 71: 219-235.
16. Matousková E., Dudorkinová D., Pavlíková L., Povýsil C., Veselý P. Clonal expansion of epithelial cells from Folia Biol (Praha). 1998;44 (2):67-71.primary human breast carcinoma with 3T3 feeder layer technique.
17. Могиленских А.С., Сазонов С.В., Демидов С.М. Оптимизация условий культивирования первичной карциномы молочной железы человека. Материалы YI Петербургского международного онкологического форума «Белые ночи 2020», С-Петербург, 25-28 июня 2020 г. С. 98.
18. Могиленских А.С., Седнева-Луговец Д.А. Сравнение роста первичной культуры карциномы молочной железы в различных условиях для культивирования. Актуальные вопросы современной медицинской науки и здравоохранения. Материалы V Международной научно-практической конференции молодых учёных и студентов, посвященной 75-летию Победы в Великой Отечественной войне, 90-летию УГМУ и 100-летию медицинского образования на Урале. 2020. С. 128-132.
Авторы
Могиленских Анна Сергеевна
ФГБОУ ВО Уральский государственный медицинский университет
Аспирант 2го года обучения, специальность «Патологическая физиология»
ГАУЗ СО «Институт медицинских клеточных технологий»
Научный сотрудник
Российская Федерация, 620028, г.Екатеринбург, ул. Репина, 3
Российская Федерация, 620026, г. Екатеринбург, ул. Карла Маркса, 22 annasajler@yandex.ru
Сазонов Сергей Владимирович
ФГБОУ ВО Уральский государственный медицинский университет
Заведующий кафедрой гистологии, доктор медицинских наук, профессор
ГАУЗ СО «Институт медицинских клеточных технологий»
Заместитель главного врача по науке
Российская Федерация, 620028, г.Екатеринбург, ул. Репина, 3
Российская Федерация, 620026, г. Екатеринбург, ул. Карла Маркса, 22
Седнева-Луговец Даяна Владимировна
ГАУЗ СО «Институт медицинских клеточных технологий»
Научный сотрудник
Российская Федерация, 620026, г. Екатеринбург, ул. Карла Маркса, 22
Демидов Сергей Михайлович
ФГБОУ ВО Уральский государственный медицинский университет
Заведующий кафедрой онкологии и лучевой диагностики, доктор медицинских наук, профессор
ГАУЗ СО «Институт медицинских клеточных технологий»
Ведущий научный сотрудник
Российская Федерация, 620028, г.Екатеринбург, ул. Репина, 3
Российская Федерация, 620026, г. Екатеринбург, ул. Карла Маркса, 22

