Доклиническая оценка эффективности разрабатываемого биоинженерного средства для терапии недостаточности функций печени
УДК 616.36-003.93
С.В. Костюкова 1, 2, А.В. Коротков 1, 2, Д.А. Сичкар 1, 2, Е.А. Шуман 1, 2, М.А. Десятова 1, О.Г. Макеев 1, 2
1 ГАУЗ СО Институт медициских клеточных технологий г. Екатеринбург, Российская Федерация;
2 ФГБОУ ВО Уральский государственный медицинский университет, г. Екатеринбург, Российская Федерация
УДК 616.36-003.93
Резюме. Цель исследования — получение убедительных данных об эффективности применения мультипотентных мезенхимальных стромальных клеток (ММСК), трансфецированных плазмидным вектором с геном фактора роста гепатоцитов (HGF), а также сфероидов из ММСК, трасфецированных тем же вектором (СФММСК). Материалы и методы. Морфологические и морфометрические исследования проводили на крысах линии Вистар (n=54) через 30 и 90 суток после трансплантации взвеси трансфецированных ММСК и клеточных сфероидов. Полученные результаты статистически обрабатывали. Результаты. Показаны позитивные изменения исследуемых параметров в динамике наблюдения. Так, терапия с введением взвеси трансфецированных ММСК и СФММСК по числу двуядерных клеток, толщине соединительнотканных перегородок значимо отличались от соответствующих показателей в контрольной группе.
Ключевые слова: цирроз печени, мультипотентные мезенхимальные стромальные клетки, трансдифференцировка, генотерапия, фактор роста гепатоцитов
Конфликт интересов отсутствует.
Контактная информация автора, ответственного за переписку:
Макеев Олег Германович
larim@mail.ru
Дата поступления 26.11.2020 г.
Образец цитирования:
Костюкова С.В., Коротков А.В., Сичкар Д.А., Шуман Е.А., Десятова М.А., Макеев О.Г. Доклиническая оценка эффективности разрабатываемого биоинженерного средства для терапии недостаточности функций печени. http://vestnikural.ru/article/1142. [Электронный ресурс] Вестник уральской медицинской академической науки. 2020, Том 17, №3, с. 233–242, DOI: 10.22138/2500-0918-2020-17-3-233-242
Введение
Недостаточность функций печени и ее цирроз — широко распространенная патология. Так, в России, каждый четвертый пациент стационара (независимо от профиля) имеет ту или иную степень выраженности недостаточности функции печени. Ежегодно до полутора тысячам человек ставится диагноз цирроза печени. В других странах значения заболеваемости данной патологией близки к внутрироссийским, а смертность от цирроза печени составляет порядка 30 случаев на 100 000 населения [1].
Безальтернативным методом лечения больных с завершающей стадией цирроза печени, является ее трансплантация. При этом, глобальной проблемой остается дефицит донорских органов. Так, только один из десяти пациентов, находящихся в «листе ожидания», получает такую помощь. А число ожидающих трансплантацию неуклонно возрастает [2]. В свою очередь, сложности с переживаемостью трансплантируемого органа и продолжительностью его доставки обуславливают выживаемость трансплантата в пределах 65%. Поэтому значительное количество исследовательских коллективов привлечено к разработке нетрансплантационных методов лечения как недостаточности функций, так и цирроза печени, как крайней степени развития данной патологии [3, 4]. Принимая во внимание физиологические особенности регенерации печеночной ткани, отсутствие доказанной информации о существовании печеночных стволовых клеток, а также вовлеченности в процесс восстановления целостности данного органа практически всех функционально сохранных гепатоцитов, большое внимание привлекает возможность трансплантации стволовых клеток. Предполагается, что вводимые клетки будут дифференцироваться или трансфифференцироваться (при использовании стволовых клеток другого зародышевого листка) в клетки печеночной ткани. Между тем, доля транспалантированных клеток, подвергающихся перепрограммированию в естественных условиях чрезвычайно мала и едва достигает десятых долей процента. Тем не менее данный подход считается перспективным в отношении лечения цирроза печени [5].
Таким образом, целью работы являлось подтверждение эффективности разрабатываемого средства, предусматривающего применение перепрограммированных мультипотентных мезенхимальных стромальных клеток (ММСК), трансфецированных плазмидным вектором с геном фактора роста гепатоцитов (HGF), а также сфероидов из ММСК, трасфецированных тем же вектором (СФММСК).
Материалы и методы
Для оценки влияния трансплантации преддиференцированных ММСК, а также сфероидов данных клеток при цирротическом повреждении печени привлекали линейных лабораторных крыс (Wistar) n=54. Работа проводилась на основании одобрения дизайна исследования локальным этическим комитетом Уральского госмедуниверситета МЗ РФ, а также руководствуясь Европейской конвенцией по защите позвоночных животных (Страсбург, 18.03.1986г.) и Приказом Минздрава РФ (199н, 01.04.2016 г.).
Для моделирования поражения печени у лабораторных животных применяли известную методику, сочетающую два подхода к патологии данного органа. Крысам внутрибрюшинно вводили 50%-ный раствор четыреххлористого углерода на растительном масле из расчета 0,25 мл чистого ССl4 2 раза в неделю. Кроме четыреххлористого углерода использовали раствор тиоцитамида 150 мг/кг в неделю. Последний обеспечивает улучшенное поступление четыреххлористого углерода в гепатоциты. Такой метод позволяет достичь стабильного выхода цирроза печени практически у 100% экспериментальных животных.
По формированию цирроза печени введение прекращали и животных подразделяли на 3 группы: две экспериментальные и контрольную. Для выполнения процедуры клеточной терапии использовали образцы жировой ткани пахового пояса интактных крыс в связи с присутствием в данной ткани наименее дифференцированных и функционально активных мезенхимальных стволовых клеток [6]. Забор жировой ткани осуществлялся под внутривенной анестезией.
Выделение и культивирование ММСК из жировой ткани проводили по стандартной методике [7].
В качестве основы вектора нами была использована pBABE-puro (Addgene plasmid 176). Синтез ДНК, кодирующей HGF, осуществлялся путем обратной транскрипции с использованием набора RTS (Promega). Праймеры для ПЦР сконструированы с использованием данных и программ, расположенных на сайте NCBI. Клетки снимали с флаконов с использованием раствора трипсина — Версена 0,2% и 0,25% соответственно (Sigma Aldrich). Снятые клетки помещали в 25-сантиметровые матрасы и культивировали в инкубаторе при 5% СО2 в среде DMEM/F12 с фетальной бычьей сывороткой от 3 до 12%, что определялось степенью дифференцированности клеточной культуры. На начальном этапе клетки культивировали с добавлением пенициллина, стрептомицина и тилозина в «культуральных» концентрациях. Смену среды производили каждые 3 дня.
По достижению 70% конфлюентности клетки трансфецировали pBABE-puro HGF (Addgene) с использованием набора Lipofectamine™ 2000 (Invitrogen) согласно протоколу изготовителя. Через 24 часа клетки отмывали от свободного плазмидного вектора и трансфецирующей среды.
Трансфекция дала возможность получить из мультипотентных мезенхимальных стромальных клеток жировой ткани клетки с фенотипическими признаками гепатоцитов.
ММСК крысам вводили в воротную вену путем внутрипортальной инъекции.
По завершении 30 и 90 дней после введения клеток (или физраствора контрольной группе животных) животных подвергали эвтаназии (посредством воздушной эмболии), что позволило исследовать относительно отдаленные результаты терапии. Для исследования выделенной печени осуществляли микроскопическое исследование пораженной ткани [8] с окраской гематоксилин-эозин.
Морфометрию проводили на микроскопе Olympus СX-41 с использованием пакета специальных программ в 10 полях зрения при увеличении от 100 до 300 [9]. Исследовали количество двух- и более ядерных клеток, степень дистрофических изменений и толщину соединительнотканных междолевых перегородок [10].
Результаты обрабатывали с использованием критериев Манна-Уитни, Краскела-Уоллиса и xi-квадрата Пирсона. Расчеты производились с использованием пакета STATISTICA 8.0. Значимыми считали результаты при р<0,05.
Таблица 1
Дизайн исследования
Экспериментальная группа | Характеристика группы |
Группа 1 экспериментальная группа №1(n=18) | По завершению моделирования цирроза печени крысам продолжали внутрибрюшинное введение физиологического раствора в эквивалентном контролю количестве на протяжении 6 дней. На 7день осуществляли внутрипортальное однократное введение суспензии трансфецированных ММСК из расчета 5×106/кг массы животного (106клеток для 200-граммовой крысы) в 0,5 мл физраствора. |
Группа 2 экспериментальная группа №2 (n=18) | По завершению моделирования цирроза печени крысам продолжали внутрибрюшинное введение физиологического раствора в эквивалентном контролю количестве на протяжении 6 дней. На 7день осуществляли внутрипортальное однократное введение суспензии сфероидов из трансфецированных ММСК из расчета 5×106/кг массы животного (106 клеток для 200-граммовой крысы) в 0,5 мл физраствора. |
Группа №3 контрольная группа (n=18) | У животных моделировали цирроз печени и ежесуточно вводили физраствор (0,2 мл) 6 раз внутрибрюшинно и седьмой (0,5 мл) — внутрипортально. Животным не проводили каких-либо терапевтических воздействий. Результаты исследования данной группы применяли в качестве объекта сравнения с животными экспериментальных групп. |
Результаты исследования
Введение четыреххлористого углерода и тиоацетамида сопровождалось возникновением цирроза печени. Визуально орган был увеличен, уплотнен, с закругленными краями и появлением бугристости.
Среди типичных признаков, наблюдающихся в печени при циррозе, отмечалось появление округлой формы незаполненных полостей, отека, пигментации, гиперемии кровеносных сосудов, лизиса эритроцитов, а также повышение количества двуядерных клеток с признаками некроза и дистрофии.
Важным признаком, отмечаемым при микроскопии, является фиброз печеночной ткани с образованием ложных долек за счет разрастания соединительнотканных перегородок.
Среднее значение толщины соединительнотканных перегородок в 3-й группе не превышало 35,12 мкм, в1-й группе — не более 34,48 мкм и во 2-й группе — 33,60 мкм. Значимых отличий между показателями отдельных групп найдено не было.
Среднее значение клеточности (двуядерные/многоядерные клетки, количество в поле зрения) в 3-й контрольной группе составляло 12,0 (11,7-12,5), в 1-й группе — 11,8 (11,3-12,3) и во 2-й группе — 11,6 (11,4-11,8), что также не позволило найти статистических различий.
Оценку степени развития признаков дистрофии после воспроизведения модели цирротической печени во всех трех исследованных группах также не позволила выявить значимых статистических различий.
Гистологический анализ образцов печени через 30 дней после введения трансфецированных ММСК в опытных группах выявил статистически достоверные отличия с контрольной группой.
Так, в контрольной группе (группа №3) определено равномерное расположение двуядерных/многоядерных клеток, наличие фиброзирующего процесса стромальной ткани, дистрофических изменений в гепатоцитах.
В группе 1 гистологические исследования позволили выявить некоторое количество дву- и более ядерных клеток, разрастание соединительнотканных образований, а также наличие ложных долек (рисунок 1).
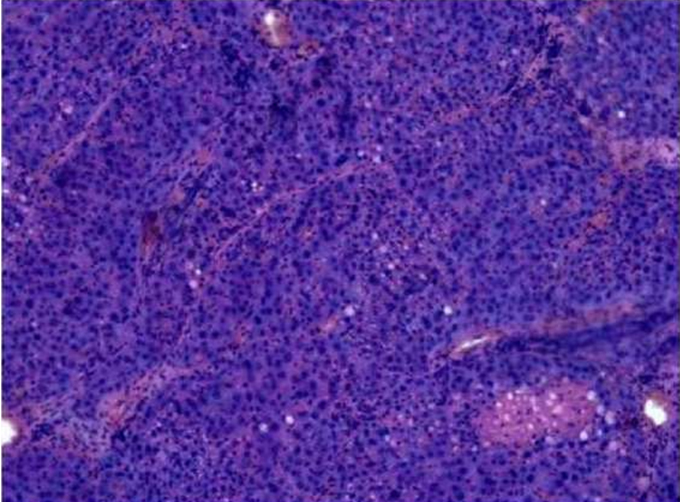
Рисунок 1. Гистологический срез печени спустя 30 дней после введения взвеси ММСК, группа 1, окраска гематокислин-эозин, увеличение ×100
В группе 2 (с введением СФММСК) через 30 дней выявлено меньшее, чем в контрольной группе число дву- и более ядерных клеток, участки умеренной дистрофии и утончение межклеточных и межлакунарных соединительнотканных перегородок (рисунок 2).
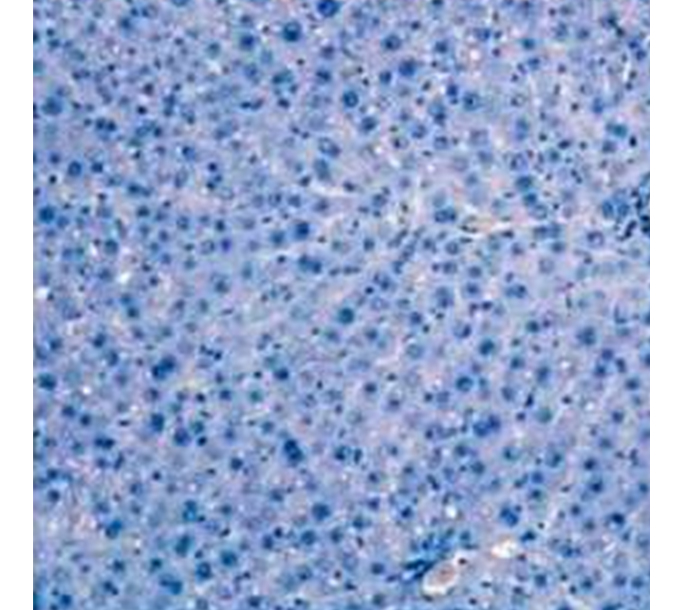
Рисунок 2. Гистологический срез печени спустя 30 дней после введения СФММСК, группа 2, окраска гематокислин-эозин, увеличение ×100
Через 30 дней после введения трансфецированных ММСК/СФММСК среднее значение толщины соединительнотканных перегородок в 3 группе составило 29,62 (28,8-30,7) мкм, в 1-й группе (с введением взвеси трансфецированных ММСК) — 22,18 (21,56-23,6) мкм и во 2-й группе 19,9 (17,8-20,5).
В контрольной группе значимость различий с опытными группами была подтверждена (р<0,05). Также различия, относимые к статистически значимым, отмечены между опытными группами.
Гепатоцитарная дистрофия в 3-й (контрольной) группе была выражена у 4-х животных и умеренно выражена у 2-х; в 1-й группе (с введением взвеси трансфецированных ММСК) и незначительно выражена у 3-х крыс; и во 2-й группе (с введением СФММСК) дистрофия наблюдалась у 2-х крыс и слабо — у 4-х.
Сравнение контрольной и опытных групп продемонстрировало наличие статистической значимости различий. Других значимых различий не выявлено.
При морфологическом и морфометрическом анализе образцов печени через 90 дней после введения трансфецированных ММСК в виде суспензии клеток или сфероидов изменения определены в качестве значимых, по сравнению с контролем.
Так, 3-я группа характеризовалась наличием слабовыраженных процессов репарации печеночной ткани. Это проявлялось в виде сохранения дистрофических изменений, фиброза структур и снижения количества двуядерных клеток.
В группе 1 при гистологическом исследовании выявлено истончение межклеточных и межлакунарных соединительнотканных перегородок с незначительной компактизацией клеток печеночных долек и маловыраженной клеточной дистрофией (рисунок 3).
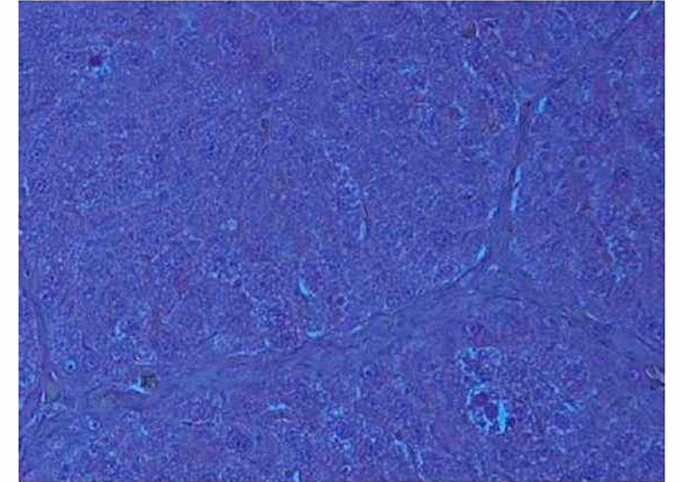
Рисунок 3. Гистологический срез печени через 90 дней после введения взвеси трансфецированных ММСК, группа 1, окраска гематокислин — эозин, увеличение ×100
Гистологические срезы печени крыс в группе 2 были наиболее приближены к нормальным значениям. По большей площади срезов выявляются остаточные явления фиброза, истончение соединительнотканных перегородок, маловыраженная дистрофия на некоторых участках. Количество дву- и многоядерных клеток не отличалось от интактных значений (рисунок 4).
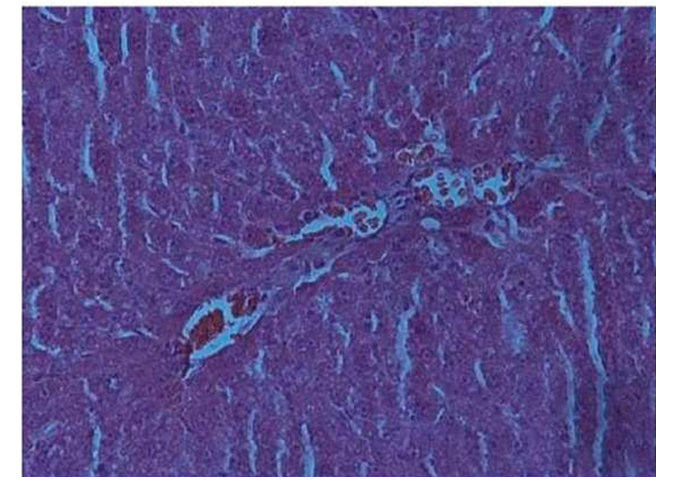
Рисунок 4. Гистологический срез печени через 90 дней после введения СФММСК, группа 2, окраска гематокислин — эозин, увеличение ×100
Среднее значение толщины соединительнотканных перегородок в 3-й группе составило 25,5 (24,68-26,11) мкм; в 1-й группе (с введением взвеси трансфецированных ММСК) — 16,76 (15,34-17,87); во 2-й группе (с введением СФММСК) — 12,89 (11,76-13,85) мкм. В 3-й группе толщина соединительнотканных перегородок достоверно превышала соответствующий показатель опытных групп. В тоже время различия выявлялись и между опытными группами (1-й и 2-й).
Признаки дистрофии печеночной ткани в 3-й группе наблюдались у 2-х животных и были слабо выражены у 4-х. В 1-й группе были слабо выражены у 1-й крысы и практически не наблюдались у 5-ти животных. Во 2-й группе признаков печеночной дистрофии практически не наблюдалось.
В 3-й группе среднее значение дву- и более ядерных клеток в одном поле зрения не превышало 11,5 (10,8-11,9), в 1-й группе — 9,0 (8,7-10,1), и во 2-й группе — 8,2 (7,9-8,7). Найдены статистические различия между показателями 1-й и 2-й групп (р=0,02).
Показатели толщины соединительнотканных перегородок у животных, при проведении клеточной терапии (группа 1) представлена на рисунке 5.
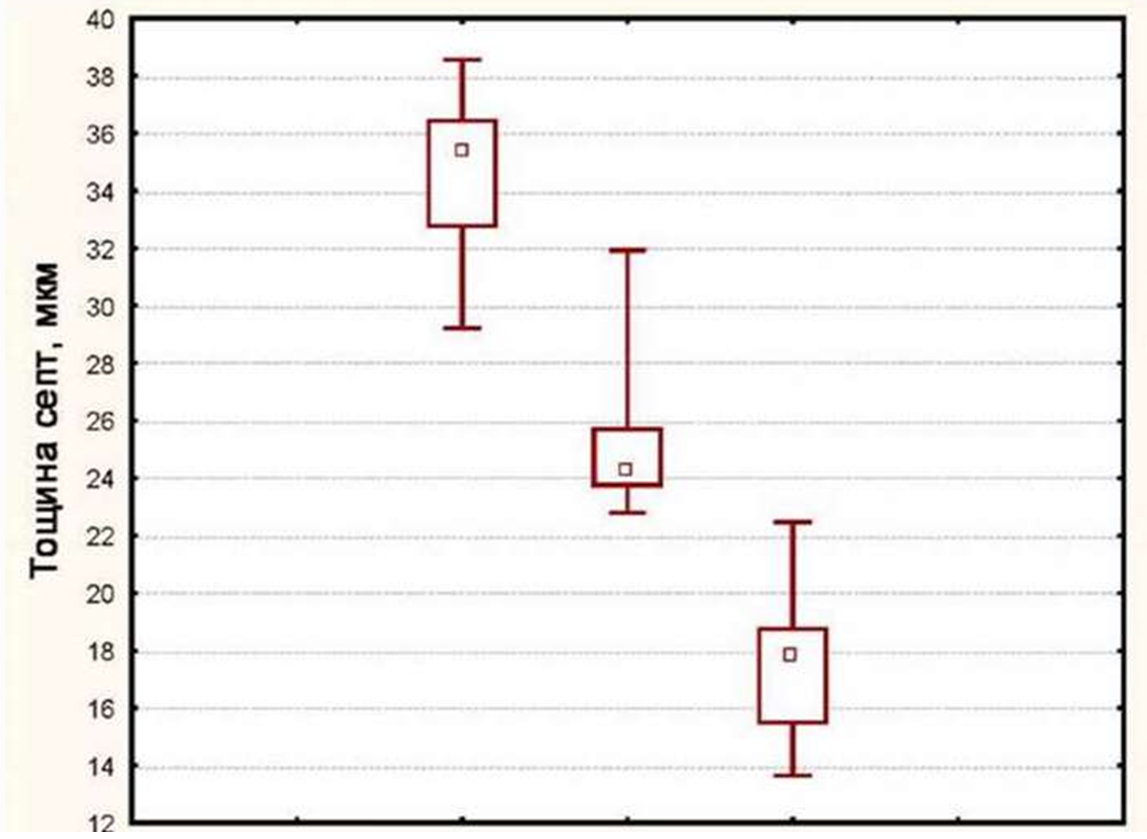
До введения ММСК; 1 месяц; 3 месяца
Рисунок 5.Динамика толщины соединительнотканных перегородок на гистологических срезах печени животных группы 1
Показатели толщины соединительнотканных перегородок у животных после введения СФММСК — (группа 2) представлена на рисунке 6.
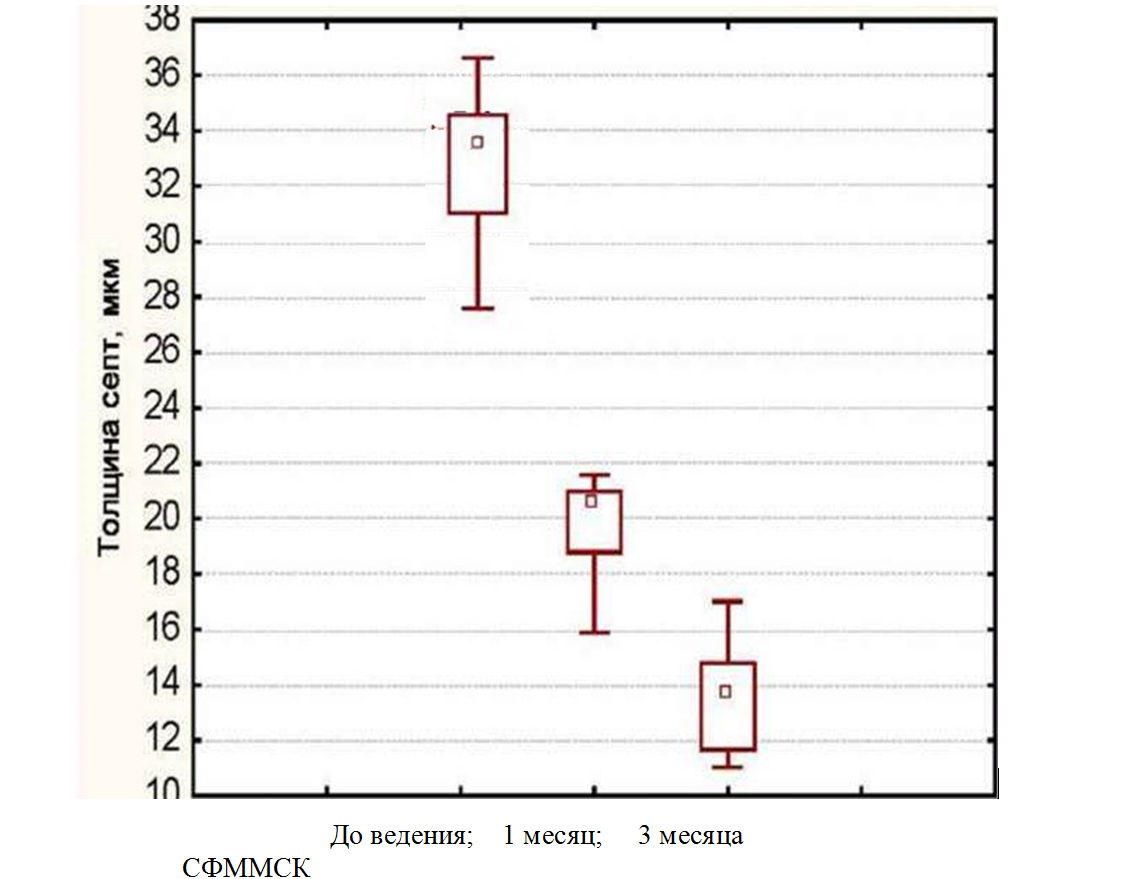
Рисунок 6. Динамика толщины соединительнотканных перегородок на гистологических срезах печени животных группы 2
Обсуждение
Исследования гистологических параметров животных после двухмесячного моделирования цирроза печени посредством введения растворов четыреххлористого углерода и тиоацетамида продемонстрировали воспроизводимость данного метода у всех 54 из 54-ти исследованных животных, условно разделенных на 3 группы — опытные и контрольную. Отсутствие статистической значимости морфологических показателей при условии стохастического разделения групп свидетельствует о стабильности данной модели, что дает основание для проведения исследования средств для терапии цирроза печени.
Спустя 30 дней после воссоздания гепатотоксической модели, а также введения взвеси трансфецированных ММСК (1 группа) и сфероидов из трансфецированных ММСК (2 группа) в сравнении с группой животных без клеточной терапии (3 группа, контроль), выявлены некоторые улучшения морфогистологических показателей, что нашло выражение в виде меньшей толщины соединительнотканных межлакунарных и межклеточных перегородок, а также признаков дистрофии и числа дву- и более ядерных гепатоцитов.
Через 90 дней наблюдаются более выраженные позитивные изменения в группах с клеточной терапией по сравнению как с исходными показателями (во всех группах), так и с соответствующими показателями контрольной группы.
Важным представляется, что у лабораторных крыс, которым вводили клеточные сфероиды, морфогистологические показатели оказались лучше, чем у крыс, которым проводилась терапия взвесью трансфецированных ММСК. Означенное находит проявление в снижении количества двуядерных клеток, а также толщины соединительнотканных перегородок.
Использование сформированных сфероидов, по-видимому, в большей степени отвечает структурно-функциональным особенностям печеночной ткани в физиологических условиях, когда послойное строение клеток различается по активности, в зависимости от удаленности от лакун.
Заключение
Введение трансфецированных плазмидным вектором (несущим в качестве полезного ген фактора роста гепатоцитов) ММСК в качестве монотерапии, а также сфероидов из трансфецированных тем же вектором ММСК, сопровождается улучшением морфогистологических параметров поврежденной печени в динамике на протяжении 90 дней после трансплантации ММСК.
Введение СФММСК сопровождается несколько лучшими показателями, чем таковые у крыс с введением взвеси ММСК.
Таким образом, избранные для исследования формы биоинженерного средства (взвесь трансфецированных ММСК и СФММСК) подтвердили эффективность в отношении терапии цирроза печени в доклинических исследованиях. При этом клеточные сфероиды по-видимому более перспективны, так как отличаются от других групп ускоренной репарацией повреждения печеночной ткани.
ЛИТЕРАТУРА
- Scaglione S., Kliethermes S., Cao G., Shoham D., Durazo R., Luke A., Volk M. L. et al. The epidemiology of cirrhosis in the United States //Journal of clinical gastroenterology. – 2015. – Т. 49. – №. 8. – С. 690-696.
- Sakai Y, Takamura M, Seki A, et al. Phase I clinical study of liver regenerative therapy for cirrhosis by intrahepatic arterial infusion of freshly isolated autologous adipose tissue-derived stromal/stem (regenerative) cell. Regen Ther. 2017;6:52‐64. Published 2017 Mar 9. doi:10.1016/j.reth.2016.12.001.
- Mahmood A, Seetharaman R, Kshatriya P, Patel D, Srivastava AS. Stem Cell Transplant for Advanced Stage Liver Disorders: Current Scenario and Future Prospects [published online ahead of print, 2019 Oct 4]. Curr Med Chem. 2019;10.2174/0929867326666191004161802. doi:10.2174/0929867326666191004161802
- Alt EU, Winnier G, Haenel A, et al. Towards a Comprehensive Understanding of UA-ADRCs (Uncultured, Autologous, Fresh, Unmodified, Adipose Derived Regenerative Cells, Isolated at Point of Care) in Regenerative Medicine. Cells. 2020;9(5):E1097. Published 2020 Apr 29. doi:10.3390/cells9051097
- Cho K.A., Ju S.Y., Cho S.J., Jung Y.J., Woo S.Y., Seoh J.Y. et al. Mesenchymal stem cells showed the highest potential for the regeneration of injured liver tissue compared with other subpopulations of the bone marrow //Cell Biology International. – 2009. – Т. 33. – №. 7. – С. 772-777.
- Parola M., Robino G. Oxidative stress-related molecules and liver fibrosis // Journal of hepatology. — 2001. — Т. 35. — №. 2. — С. 297-306.
- Nahon P, Ganne-Carrié N. Management of patients with pre-therapeutic advanced liver fibrosis following HCV eradication. JHEP Rep. 2019;1(6):480‐489. Published 2019 Nov 18. doi:10.1016/j.jhepr.2019.11.001.
- Mesenchymal stem cells showed the highest potential for the regeneration of injured liver tissue compared with other subpopulations of the bone marrow / K. A. Cho [et al.] // Cell. Biol. Int. 2009 Jul. Vol. 33, N 7. P. 772-777.
- Zuk P.A., Zhu M., Ashjian P., De Ugarte D.A., Huang J.I., Mizuno H., Hedrick M.H. et al. Human adipose tissue is a source of multipotent stem cells // Molecular biology of the cell. — 2002. — Т. 13. — №. 12. — С. 4279-4295.
- Collan Y. Morphometry in pathology: another look at diagnostic histopathology. Pathol Res Pract. 1984;179(2):189 192. doi:10.1016/S0344-0338(84)80126-0
- Kesten S, Fraser JK. Autologous Adipose Derived Regenerative Cells: A Platform for Therapeutic Applications. Surg Technol Int. 2016;29:38‐44.
- Lockhart RA, Aronowitz JA, Dos-Anjos Vilaboa S. Use of Freshly Isolated Human Adipose Stromal Cells for Clinical Applications. Aesthet Surg J. 2017;37(suppl_3):S4‐S8. doi:10.1093/asj/sjw270/
Авторы
КостюковаСветланаВладиленовна
ГАУЗ СО Институт медицинских клеточных технологий
ФГБОУ ВО Уральский государственный медицинский университет
К.б.н., ведущий научный сотрудник
Российская Федерация, 620026, Екатеринбург, ул. Карла Маркса, д. 22 а
svkostukova@mail.ru
Коротков Артем Владимирович
ГАУЗ СО Институт медицинских клеточных технологий
ФГБОУ ВО Уральский государственный медицинский университет, г. Екатеринбург, РФ
К.м.н., ведущий научный сотрудник
Российская Федерация, 620026, Екатеринбург, ул. Карла Маркса, д. 22 а
akorotkov64@mail.ru
Сичкар Дарья Александровна
ГАУЗ СО Институт медицинских клеточных технологий
ФГБОУ ВО Уральский государственный медицинский университет
Младший научный сотрудник
Российская Федерация, 620026, Екатеринбург, ул. Карла Маркса, д. 22 а
Sichkar2017@yandex.ru
Шуман Евгений Александрович
ГАУЗ СО Институт медицинских клеточных технологий
ФГБОУ ВО Уральский государственный медицинский университет
Научный сотрудник
Российская Федерация, 620026, Екатеринбург, ул. Карла Маркса, д. 22 а
evgenyshuman@gmail.com
Десятова Мария Анатольевна
ФГБОУ ВО Уральский государственный медицинский университет
Младший научный сотрудник
Российская Федерация, 620109, Екатеринбург, ул. Ключевская, 17, оф. 304/305
mardesyatova03@yandex.ru
Макеев Олег Германович
ГАУЗ СО Институт медицинских клеточных технологий
ФГБОУ ВО Уральский государственный медицинский университет
Д.м.н., профессор, главный научный сотрудник
Российская Федерация, 620026, Екатеринбург, ул. Карла Маркса, д. 22 а
larim@mail.ru

