Антигипергликемический эффект экстрактов северных ягод на модели сахарного диабета II типа у крыс, инициированного стрептозотоцином
УДК 599.32:591.2+616.379-008.64+615.322
Е.А. Кривых ¹, А.Е. Гуляев ², Л.В. Коваленко ³, З.Т. Шульгау ⁴
¹ БУ ВО Ханты-Мансийского автономного округа – Югры «Ханты-Мансийская государственная медицинская академия», г. Ханты-Мансийск, Российская Федерация;
² Частное учреждение «National Laboratory Astana» Назарбаев университет, г. Нур-Султан, Республика Казахстан;
³ БУ ВО Ханты-Мансийского автономного округа – Югры «Сургутский государственный университет», г. Сургут, Российская Федерация;
⁴ Республиканское государственное предприятие «Национальный центр биотехнологии», г. Нур-Султан, Республика Казахстан
Резюме. Целью данного исследования явилось изучение потенциальных терапевтических свойств водно-спиртовых экстрактов черники, голубики, брусники, клюквы, на модели экспериментального стрептозотоцинового сахарного диабета. Материал и методы исследования. Для получения полифенольных водно-спиртовых экстрактов северных ягод использовали дикорастущую клюкву, чернику, бруснику, голубику, собранную в летне-осенний период 2018 года в Сургутском районе Ханты-Мансийского округа Тюменской области Российской Федерации. Концентрирование экстрактов проводили в вакуумном испарителе до уровня полифенолов в 10 мг/мл. Крысам вводили полифенольные экстракты из расчета 10 мг/кг (вводимый объем 0,2-0,3 мл). Результаты. Концентрацию полифенолов в образцах исследовали, используя коммерческий набор для определения концентрации полифенолов «Polyphenols folin-ciocalteu (ENOLOGY line by BioSytems. Spain)», в соответствии с инструкцией производителя реагента. Результаты выражали в эквиваленте галловой кислоты, т.е. мг галловой кислоты/мл ягодного экстракта (mgGAE /ml). Заключение. На модели сахарного диабета II типа, полученного у крыс при введении стрептозотоцина, исследовано влияние экстрактов дикорастущих ягод клюквы, брусники, черники и голубики Северо-Западной Сибири на уровень гликемии и инсулинорезистентности, показатели липидного обмена, уровень экспрессии CRP, IL-6 и TNF-α в печени и жировой ткани крыс, также установлены гистопатологические изменения в ткани поджелудочной железы. Определено, что экстракты черники, клюквы, брусники и голубики на модели диабета снижают выраженность инсулинорезистентности наподобие метформина, снижают уровень гликемии (кроме экстракта брусники), снижают концентрацию триглицеридов (кроме экстракта брусники), уменьшают концентрацию ЛПНП (кроме брусники и клюквы). Использование на фоне диабета экстракта черники снижает экспрессии генов воспалительных цитокинов IL-6, TNF-α и CRP. При этом в плазме крови экстракты северных ягод препятствуют избыточному выбросу свободных радикалов и повышают антиоксидантную активность. Патоморфологические исследования ткани поджелудочной железы документируют меньшую степень повреждения островков Лангерганса на фоне введения экстрактов северных ягод.
Ключевые слова: модель диабета, стрептозотоцин, экстракты клюквы, брусники, черники, голубики, гликемия, инсулинорезистентность, триглицериды, ЛПНП оксидативный статус, гистология ткани поджелудочной железы
Конфликт интересов отсутствует.
Контактная информация автора, ответственного за переписку:
Кривых Елена Алексеевна
KrivyhEA@hmgma.ru
Дата поступления 04.03.2020 г.
Образец цитирования:
Кривых Е.А., Гуляев А.Е., Коваленко Л.В., Шульгау З.Т. Антигипергликемический эффект экстрактов северных ягод на модели сахарного диабета II типа у крыс, инициированного стрептозотоцином. Электронный ресурс http://vestnikural.ru/article/1138. Вестник уральской медицинской академической науки. 2020, Том 17, №3, с. 193–205, DOI: 10.22138/2500-0918-2020-17-3-193-205
Введение
Принято относить сахарный диабет к категории болезней оксидативного стресса и хронического течения воспалительного процесса [1]. Окислительный стресс, сопровождающийся усилением свободнорадикальных процессов и снижением функционирования эндогенной антиоксидантной системы, является, видимо, важным патофизиологическим звеном развития осложнений при сахарном диабете [2, 3].
На этом фоне поиск новых биологически активных веществ, способных проявлять комплексную активность на основе универсального антиоксидантного и противовоспалительного механизма действия не теряет актуальности.
Представляет большой научный и практический интерес расширение объема экспериментальных исследований с целью доказательства гипогликемической и антиоксидантной активности индивидуальных веществ и экстрактов, содержащих фенольные соединения, на различных моделях in vivo, из которых наиболее информативной является модель сахарного диабета.
Наибольшее распространение в современной экспериментальной диабетологии получили химические модели сахарного диабет, чаще всего модель сахарного диабета у экспериментальных животных получают, используя стрептозотоцин [4]. Относительно механизма действия стрептозотоцин известно, что одной из основных причин, вызывающих токсическое поражение ß-клеток многие авторы называют образование гидроксильных радикалов [5]. Эти гидроксильные радикалы и считают в конечном итоге ответственными за гибель β-клеток, имеющих особенно низкую антиоксидантную защитную способность, и последующее развитие диабета.
Как источник полифенолов — антиоксидантов более изучена культивируемые черника (Vaccinium myrtillus) и, существенно меньше, клюква (Vaccinium erythrocarpum) в северо-американском и северо-европейском вариантах [6,7]. Относительно других северных ягод сведений крайне мало, а эффекты на моделях диабета описаны недостаточно.
Для уточнения возможности влияния экстрактов северных ягод региона Северо-Западной Сибири на углеводный и липидный обмен эксперимент был проведен на модели сахарного диабета II типа, полученной с помощью стрептозотоцина.
Целью данного исследования явилось изучение потенциальных терапевтических свойств водно-спиртовых экстрактов черники, голубики, брусники, клюквы, на модели экспериментального стрептозотоцинового сахарного диабета.
Материал и методы исследования
Для получения полифенольных водно-спиртовых экстрактов северных ягод использовали дикорастущую клюкву, чернику, бруснику, голубику, собранную в летне-осенний период 2018 года в Сургутском районе Ханты-Мансийского округа Тюменской области Российской Федерации. Концентрирование экстрактов проводили в вакуумном испарителе до уровня полифенолов в 10 мг/мл. Крысам вводили полифенольные экстракты из расчета 10 мг/кг (вводимый объем 0,2-0,3 мл). Концентрацию полифенолов в образцах исследовали, используя коммерческий набор для определения концентрации полифенолов «Polyphenols folin-ciocalteu (ENOLOGY line by BioSytems. Spain)», в соответствии с инструкцией производителя реагента. Результаты выражали в эквиваленте галловой кислоты, т.е. мг галловой кислоты/мл ягодного экстракта (mgGAE /ml).
В работе были использованы крысы Wistar, самцы в возрасте 7-8 месяцев, массой тела 210-230 гг. Они были размещены в клетках при комнатной температуре (22±2) °С с 12-часовым циклом свет/темнота и минимальной относительной влажности 40%. Крыс кормили стандартным гранулированным кормом и доступ к воде был свободным, ad libitum.
Экспериментальные исследования проводились в соответствии с Правилами лабораторной практики в Российской Федерации. Приложение утверждено приказом Министерства Здравоохранения Российской Федерации от 19.06.2003 № 267, а также Европейской Конвенциией о защите позвоночных животных, используемых для экспериментов или в иных научных целях (Страсбург, 18 марта 1986 г.) ETS N 123.
Моделирование сахарного диабета II типа (СД2) [8]. 50 крыс самцов Wistar кормили коммерческим вариантом сухого гранулированного корма с повышенным содержание жиров (El-Gomhoria Company, Cairo, Egypt). В качестве источника избыточного количества углеводов использовали 10%-ный раствор фруктозы вместо питьевой воды в течение 4 недель.
Таблица 1
Состав диеты с повышенным содержанием жиров (г/кг)
Ингредиенты | Диета с повышенным содержанием жиров AIN-76A diet #100496 |
Casein | 200 |
DL-Метионин | 3 |
Corn Statch | 150 |
Sucrose | 345 |
Cellulose | 50 |
Corn Oil | – |
Beef Tallow | 205 |
Salt Mixture | 35 |
Vitamine Mixture | 10 |
Choline Bitartrate | 2 |
Fat % (Calories) | 40 |
Далее, через 4 недели все животным внутрибрюшинно ввели по 45 мг/кг стрептозотоцина в 0,2 М растворе натрия фосфата (pH 4,5), дважды через 3 дня. Стрептозотоцин вводили крысам после 12-часового голодания. Через 3 дня после последней инъекции стрептозотоцина оценивали уровень глюкозы в крови, взятой из хвостовой вены крысы, на приборе для измерения уровня глюкозы крови «Gamma Mini» (Gamma, Великобритания). Основной критерий включения крыс в экспериментальную группу — уровень глюкозы крови более 15 мМоль/л, таковых оказалось 33 головы. Для получения лечения в течение 6 дней (недели) были сформированы следующие группы животных: a) интактные (n=3) b) контроль (модель диабета) получавшие ежедневно по 0,5 мл воды интрагастрально, n=5; c) группа сравнения, получавшие ежедневно 300 мг/кг метформина (в виде суспензии в 0,5 мл воды) интрагастрально, n=5; d) группа, получавшая экстракт клюквы ежедневно по 0,5 мл интрагастрально, n=6; e) группа, получавшая экстракт брусники ежедневно по 0,5 мл интрагастрально, n=6; f) группа, получавшая экстракт черники ежедневно по 0,5 мл интрагастрально. n=6; g) группа, получавшая экстракт голубики ежедневно по 0,5 мл интрагастрально, n=5.
Во всех экспериментах присутствовали интактные крысы, такого же возраста, массы тела и пола, как и участвующие в моделировании.
Через 24 часа после окончания периода моделирования проведен тест толерантности к инсулину для подтверждения наличия диабета II типа. Тест толерантности к инсулину выполняли следующим образом. Раствор кристаллического инсулина (30 МЕ/100 г массы тела, LILLY) вводили подкожно. Образцы крови собирали через 30, 60 и 120 мин. в пробирки с гепарином, и 25 мкл аликвоты были использованы для определения концентрации глюкозы глюкозо-оксидазным методом. Одного разреза на кончике хвоста было достаточно, чтобы собрать все образцы крови. На графике концентрация/время строили фармакокинетическую кривую глюкозы в крови. С помощью компьютерной программы Bordgia 1.03 рассчитывали AUC (интегральная площадь под фармакокинетической кривой), по методу наименьших квадратов проводили анализ кривой содержания глюкозы в крови от 0 до 120 минут [9].
Уровень глюкозы определяли через 72 часа после введения аллоксана и на шестые сутки от начала введения исследуемых экстрактов в крови, взятой из хвостовой вены, на приборе для измерения уровня глюкозы крови «Gamma Mini» (Gamma, Великобритания).
При исследовании уровня экспрессии CRP, IL-6 и TNF-α крыс с моделью диабета mРНК из печени и жировой ткани (паранефральный жир) выделяли, ре-транскрибировали ДНК и подвергали двухстадийной амплификации с помощью обратной транскрипционной полимеразной цепной реакции (ОТ-ПЦР) в реальном времени с использованием специфических праймеров для генов CRP, IL-6 и TNF-α с использованием мини-набора RNeasy Lipid Tissue (Qiagen # 74804) для жировой ткани, в то время как mРНК из печени выделяли с использованием мини-набора RNeasy (Qiagen # 74104). Качество и количество выделенной mРНК определяли спектрофотометрически, измеряя оптическую плотность при 260 нм и 280 нм в кюветах, прозрачных для УФ-излучения. Обратная транскрипция кДНК и удаление геномной ДНК были выполнены с использованием QuantiTect Reverse. Комплект для транскрипции (Qiagen # 205313). Продукт обратной транскрипции подвергали воздействию ОТ-ПЦР в системе количественной ПЦР (Bio-Rad CFX96) с использованием мастер-смеси Sybr Green (SSoFastEvaGreen, Bio Rad # 172-5202) и праймеров (F – прямых, R –обратных) специфичных для крыс:
TNFα-F: 5′-GGGACAGTGACCTGGACTGT-3′.
TNFα-R: 5′-TTCGGAAAGCCCATTTGAGT-3′.
IL6-F: 5′-TCTATACCACTTCACAAGTCGGA-3′.
IL6-R: 5′-GAATTGCCATTGCACAACTCTTT-3′.
CRP-F: 5′-TTCCCAAGGAGTCAGATACTTCC-3′.
CRP-R: 5′-TCAGAGCAGTGTAGAAATGGAGA-3′.
Для каждого праймера и ткани (печени или жировой ткани) анализ проводили в трех повторностях с реакционным объемом 20 мкл на лунку (SybrGreen Mix 1 ×, праймеры прямые и обратные 0,2 мкМ, продукт обратной транскрипции 1,5 мкл). После стадии активации фермента (95°C в течение 30 с), 45 циклов амплификации проводилось (денатурация при 95°С в течение 2 с, отжиг/удлинение при 60°С в течение 5 с), затем следует кривая плавления (75–95°C при увеличении на 0,5° C, 2с на шаг) для обеспечения специфики амплификации. Относительная экспрессия генов была определена методом ΔΔCt, как описано Livak и Schmittgen [10] относительно гена домашнего хозяйства (бета-актин) и выражается в виде кратной вариации по сравнению с контрольными животными.
Исследование оксидативного статуса в плазме крови крыс на 6 сутки от начала введения экстрактов проведено на приборе FRAS 4 — Free Radical Analytical System (Evolvo s.r.l., Italy) с использованием коммерческих наборов Kit REDOX, включающих D-ROMs test (показывает концентрацию активных форм кислорода (АФК) в плазме крови, исчисляется в произвольных единицах, называемых «Carratelli Units» (U. Carr)) и PAT test (характеризует общую антиоксидантную активность плазмы крови в произвольных единицах «Cornelli Unit» (U. Cor)) [11].
Для гистологического исследования были взяты образцы ткани поджелудочной железы крыс, которые фиксировали в 10% формалине при 4°С не менее 24 часов, окрашивали гематоксилином и эозином, анализировали на специализированном аппаратном компьютеризированном комплексе фирмы «Leica microsystems» на микроскопе «Leica DM 1000».
Статистический анализ. Данные были выражены как Me [min; max], где
M — медиана;
min — минимальное значение;
max — максимальное значение.
Результаты и обсуждение
Таблица 2
Результаты теста толерантности к инсулину у крыс, получавших экстракты северных ягод Me [Q1; Q3]
Группы экспериментальных животных | Интегральная площадь под кривой «концентрация-время» (AUC) глюкозы в течение времени 0–120 мин. |
Интактные крысы (n=3) | 613,7 [485,7-695,7] |
Контроль (n=5) | 1670,4 [1435,1-1815,6] |
Экстракт черники (n=6) | 1210,6 *[985,6-1415,5] |
Экстракт клюквы (n=5) | 1309,0*[1035,5-1455,5] |
Экстракт брусники (n=5) | 1495,9 *[1215,6-1515,5] |
Экстракт голубики (n=5) | 1247,0 *[885,6-1388,1] |
Метформин (n=5) | 938,4 *[698,6-1125,1] |
Примечание: * р˂0,05 в сравнении с группой контроля (плацебо).
Как видно из таблицы 2 у крыс в контроле и во всех экспериментальных группах значительно увеличивается AUC глюкозы, что может свидетельствовать о наличии выраженной инсулинорезистентности. Однако, достоверные различия с величиной AUC глюкозы получены при введении экстрактов клюквы, брусники, черники и голубики, а также препарата сравнения — метформина. Все экстракты ягод и метформин в определенной степени уменьшают AUC глюкозы, что является проявлением уменьшения выраженности инсулинорезистентности. Известно, что снижение чувствительности клеток к инсулину, проявляющееся ростом AUC глюкозы является одним из факторов, способствующих развитию СД2 [12]. Инсулинорезистентность приводит к нарушению регуляции углеводного обмена, развитию гипергликемии и воспалительного статуса в тканях, что входит в патогенез СД2 [13]. Зафиксированную в условиях наших экспериментов некоторую коррекцию инсулинорезстентности при введении экстрактов сверных ягод мы склонны рассматривать как потенциально терапевтический.
Результаты исследования влияния экстрактов черники, голубики брусники и клюквы на содержание глюкозы и некоторые показатели липидного обмена в крови крыс с экспериментальным стрептозотоциновым сахарным диабетом приведены в таблице 3. Наряду с инсулинорезистентностью, зафиксированной по данным таблицы 2, доказательством наличия адекватной модели сахарного диабета II типа служит наличие в контроле гипергликемии, повышенного содержания триглицеридов и повышенного уровня ЛПНП (таблица 3).
Как видно из представленных данных, коррекция гипергликемии в сторону уменьшения произошла как в случае введения стандартного гипогликемического препарата метформин, так и в случае применения экстрактов черники, клюквы, голубики, единственный вариант, когда уменьшение уровня гликемии не достигает статистически значимого уровня — вариант использования брусники. Следует заметить, что уровень снижения глюкозы у крыс с моделью диабета под действием экстракта черники, не отличается от снижения глюкозы, вызываемого препаратом сравнения метформином. Таким образом, водно-спиртовые экстракты клюквы, черники и голубики в условиях данной модели препятствуют гипергликемическому действию стрептозотоцина и имеют гипогликемический эффект, приближающийся по выраженности к эффекту метформина.
Снижение уровня концентрации триглицеридов в крови крыс с моделью СД2 мы нашли в случае применения экстрактов клюквы, черники и голубики (в случае использования метформина и экстракта брусники эффект снижения триглицеридов не достигает уровня достоверности). Уменьшение концентрации ЛПНП установлено нами при применении экстрактов черники и голубики. НЕ определно влияние исследуемых экстрактов на уровень общего холестерина и ЛПВП.
Вероятность снижения уровня гликемиии на моделях диабета параллельно со снижением уровня триглицеридов и липопротеидов низкой плотности при введении экспериментальным животным антоциан-содержащих субстанций сообщает ряд исследователей [14-16]. Результаты наших экспериментов, в принципе, подтверждают такую возможность для экстрактов северных ягод (преимущественно для экстрактов черники и голубики, которые могут содержать более высокие концентрации антоцианов чем клюква или брусника [17]). Есть сведения, что максимальное содержание антоцианов среди множества ягод и фруктов находится именно в экстракте черники [18].
Учитывая это обстоятельство, мы провели исследование потенциала влияния экстракта черники на биомаркеры воспаления в ткани печени и в жировой ткани крыс с моделью СД2.
Результаты исследования генетической экспрессии молекул, связанных с хроническим воспалением представлены на рисунках 1-3.
Таблица 3
Результаты исследования терапевтического влияния экстрактов северных ягод на модели сахарного диабета II типа
Параметры | Варианты исследования | ||||||
Интактные крысы n=3 | Контроль n=5 | Препарат сравнения (метформин) n=5 | Экстракт клюквы n=5 | Экстракт брусники n=5 | Экстракт черники n=5 | Экстракт голубики n=5 | |
Глюкоза, мМоль/л | 3,5[2,1-4,4] | 29,4±1,6# [25,6-31,7] | 9,1±0,8* [7,6-11,5] | 18,2 [15,6-20,1] | 22,5 [18,5-25,6] | 13,2±1,4* [8,5-15,6] | 17,2±2,0* [14,1-19,5] |
Триглицериды, мг/дл | 117,6± 20,4 [100,1-125,6] | 158,1±38,2# [148,1-177,5] | 140,5±21,8 [138,1-160,5] | 128,4±16,6* [115,6-135,5] | 148,5±18,6* [135,1-148,2] | 116,0± 22,4* [98,5-135,1] | 120, 4±27,8* [111,5-131,1] |
Холестерин, мг/дл | 109,7[91,5-115,6] | 122,9 [110,1-129,6] | 130,3 [121,6-155,1] | 129,0 [119,0-139,5] | 136,9 [128,6-144,5] | 120,8 [101,5-130,6] | 132,8 [115,6-144,5] |
ЛПНП, мг/дл | 39,6±5,1 [30,1-42,5] | 56,0 [43,0-66,5] | 46,8[41,1-50,2] | 48,3[38,5-51,1] | 40,1[35,1-45,5] | 38,8 [31,1-41,5] | 35,3[30,5-41,1] |
ЛПВП, мг/дл | 41,9 [38,8-49,5] | 34,4 [29,1-45,5] | 35,3 [21,1-45,5] | 29,6 [21,1-35,5] | 33,8 [27,6-35,5] | 39,5 [34,1-41,1] | 38,5 [31,5-41,8] |
Примечание: * р˂0,05 в сравнении с группой контроля; # р˂0,05 в сравнении с интактными животными
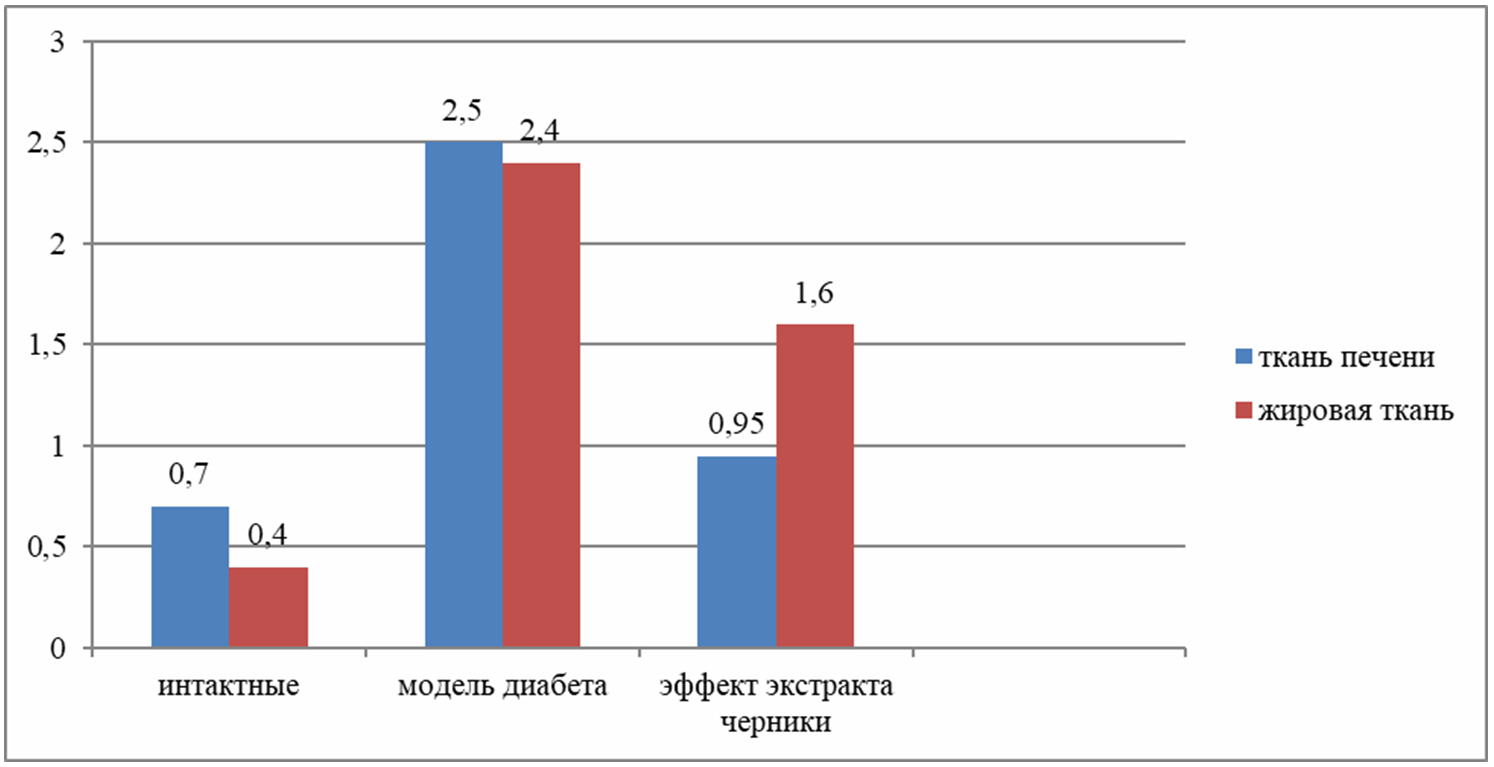
Рисунок 1. Относительная экспрессия гена IL-6, связанного с воспалением у крыс с моделью сахарного диабета (Me выраженные как 2-ΔΔCt, нормализованных к бета-актину).
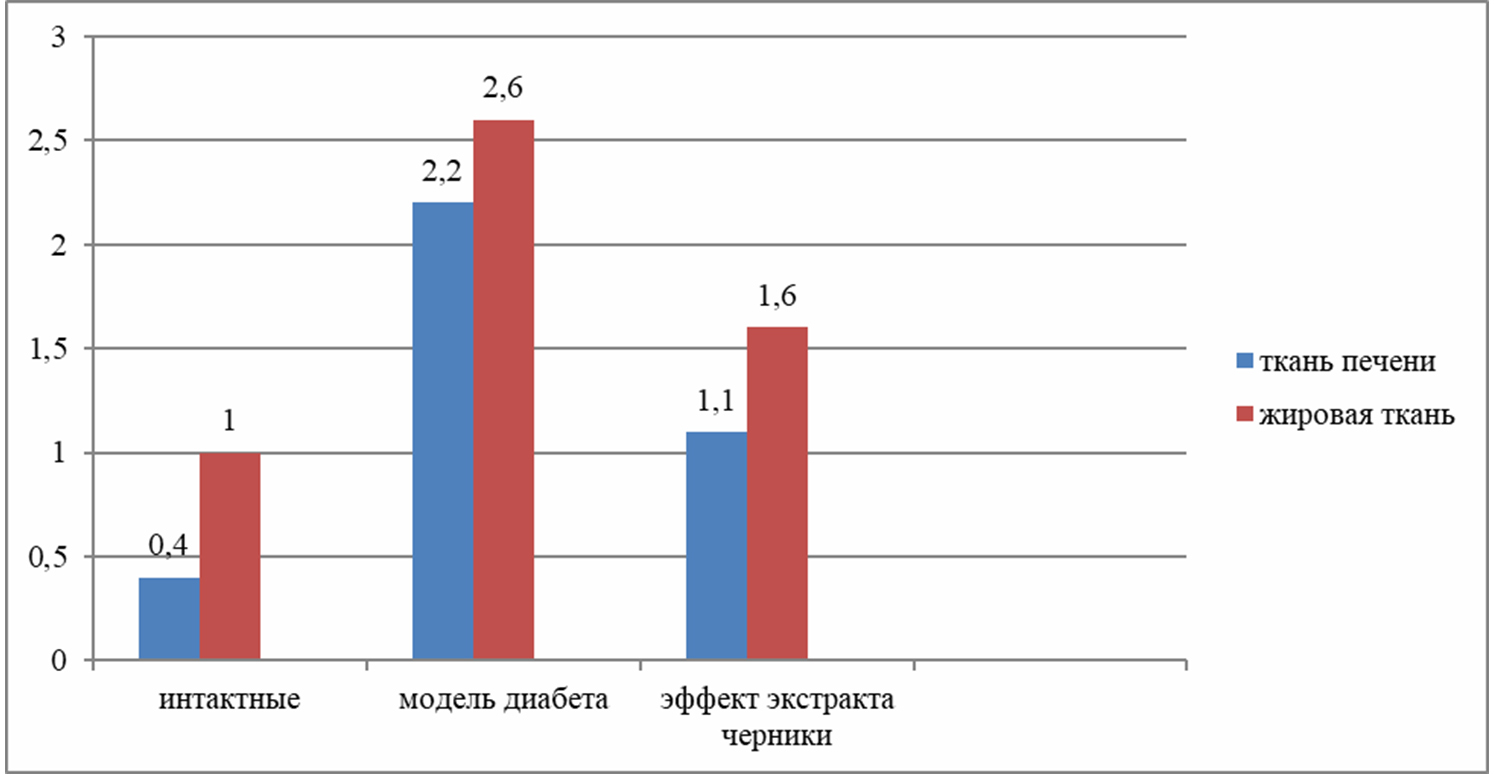
Рисунок 2. Относительная экспрессия гена TNF-α, связанного с воспалением у крыс с моделью сахарного диабета (М±s.e.m, выраженные как 2-ΔΔCt, нормализованных к бета-актину).
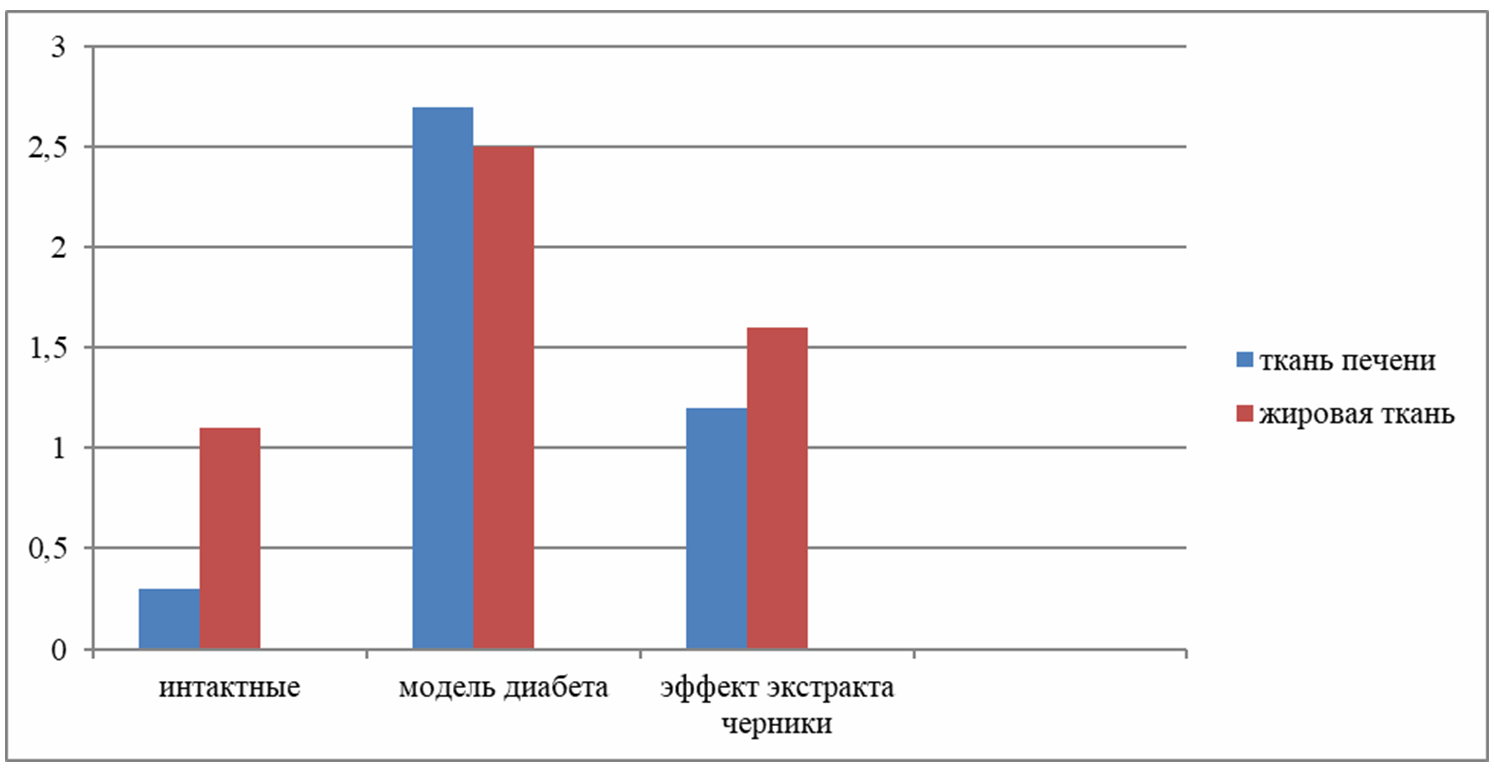
Рисунок 3. Относительная экспрессия гена CRP, связанного с воспалением у крыс с моделью сахарного диабета (М±s.e.m, выраженные как 2-ΔΔCt, нормализованных к бета- актину).
Как видно, и в ткани печени и в жировой ткани крыс с моделью диабета экспрессия IL-6, TNF-α и CRP была значительно выше, чем у интактных крыс, что подтверждает участие хронических воспалительных процессов в патофизиологии диабета II типа. Использование на фоне диабета экстракта черники дает эффект «гашения» экспрессии воспалительных генов цитокинов IL-6, TNF-α и CRP, во всех случаях уровень экспрессии статистически ниже, чем у крыс с моделью диабета в контрольной группе.
Далее мы попытались описать оксидативный статус у крыс с моделью сахарного диабета и определить вероятные эффекты исследуемых экстрактов северных ягод. Данные представлены в таблице 4.
Как видно, оксидативный статус у крыс с моделью диабета характеризовался относительно высоким уровнем концентрации свободных радикалов в плазме крови (D-ROMs test) и пониженным уровнем активности антиоксидантной системы (PAT test), что укладывается в общее представление относительно оксидативных процессов при диабете [1, 3]. Экстракты ягод клюквы, брусники, черники и голубики в этом случае уменьшали активизацию свободных радикалов и повышали антиоксидантную защиту. Экстракты черники и голубики в этом отношении кажутся более привлекательными.
Результаты этого фрагмента работы доказывают, что применение экстрактов северных ягод у крыс с моделью сахарного диабета II типа значительно и положительно влияет на биохимические и эпигенетические характеристики, уменьшая степень инсулинорезистентности, снижая уровень гликемии и нарушений липидного обмена, оксидативного стресса, экспрессии воспалительных генов и в результате, — препятствуя развитию диабета или корректируя его тяжесть.
Таблица 4
Интегральные показатели влияния экстрактов северных ягод на оксидативный статус на фоне модели диабета II типа
Группы экспериментальных животных, n | Исследуемые параметры | |
D-ROMs test, U Carr | PAT test, U Cor. | |
Интактные животные, n=5 | 395,2±31,7 355,1-415,6 | 2376±212 2111-2585 |
Животные с моделью диабета, контроль, n=6 | 911,3±81,4 788,1-1100,5 | 1836±137 1566-1988 |
Животные с моделью диабета, получавшие экстракт клюквы, n=6 | 564,3±33,1* 488,1-611,5 | 2274±159* 2100-2555 |
Животные с моделью диабета, получавшие экстракт брусники, n=6 | 582,1±44,2 499,6-650,6 | 2219±150* 1999-2488 |
Животные с моделью диабета, получавшие экстракт черники, n=6 | 318,8±25,9* 288,5-355,6 | 2405±183* 2115-2685 |
Животные с моделью диабета, получавшие экстракт голубики, n=6 | 440,0±39,5* 385,0-477,1 | 2574±203* 2288-2795 |
Примечание: * — р≥0,05 с контролем
Это же подтверждают и результаты морфологических исследований, приведенные ниже: на модели сахарного диабета II типа экстракты клюквы, черники, голубики и экстракт брусники (в меньшей степени) препятствуют повреждению структуры поджелудочной железа и островков Лангерганса в частности.
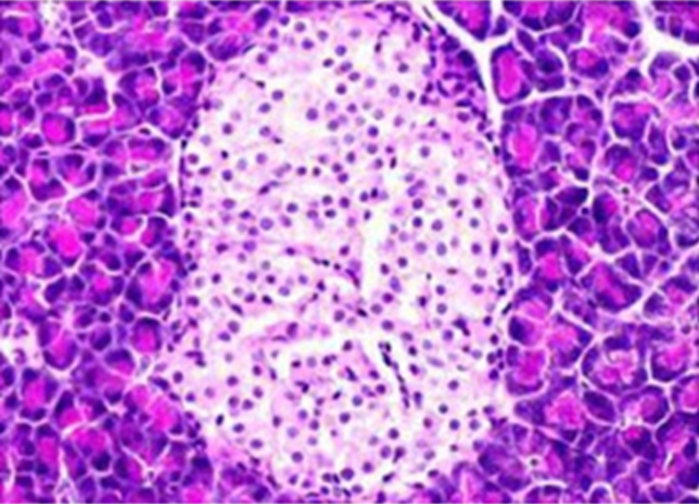
Рисунок 4. Поджелудочная железа (интактные крысы). Нормальная структура поджелудочной железы у контрольных крыс Окраска гематоксилином и эозином. Увеличение × 200.
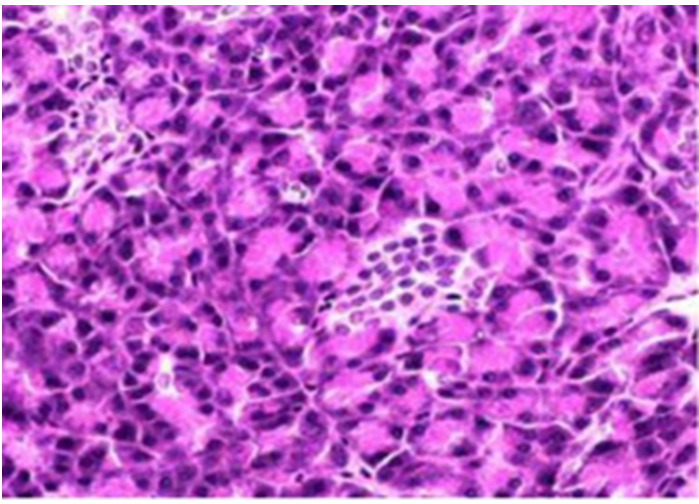
Рисунок 5. Поджелудочная железа (модель диабета). Уменьшение размера островка Лангерганса и множественная дегенерация. Окраска гематоксилином и эозином. Увеличение × 200.
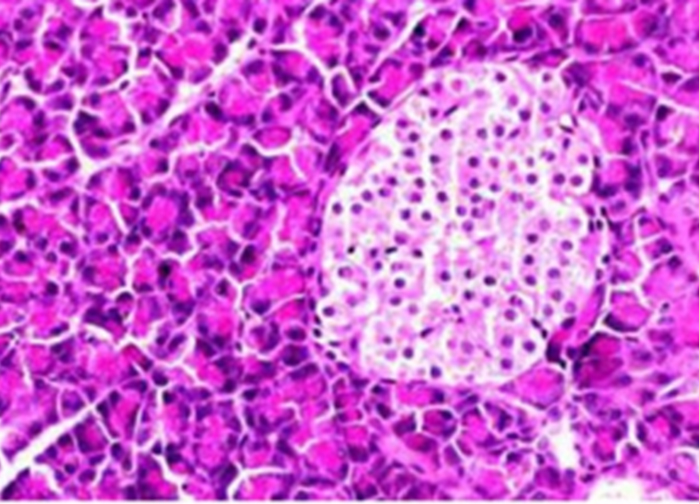
Рисунок 6. Поджелудочная железа (модель диабета, применение экстракта черники). Более сохраненная структура островка Лангерганса по сравнению с рис 2. Окраска гематоксилином и эозином. Увеличение × 200.
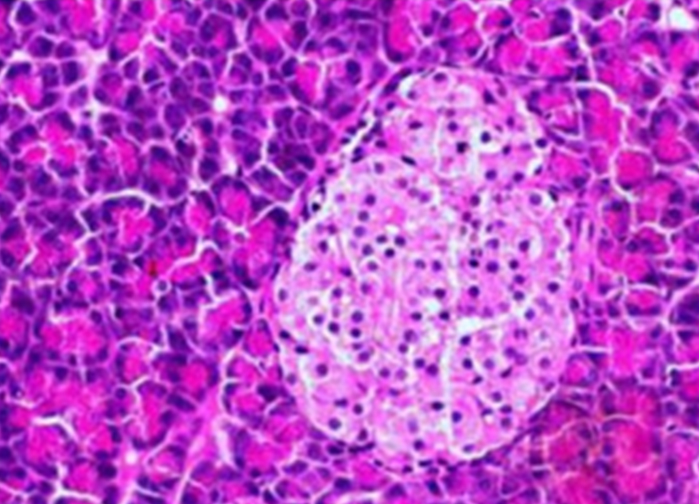
Рисунок 7. Поджелудочная железа (модель диабета, применение экстракта голубики). Более сохраненная структура островка Лангерганса по сравнению с рис 2. Окраска гематоксилином и эозином. Увеличение × 200.
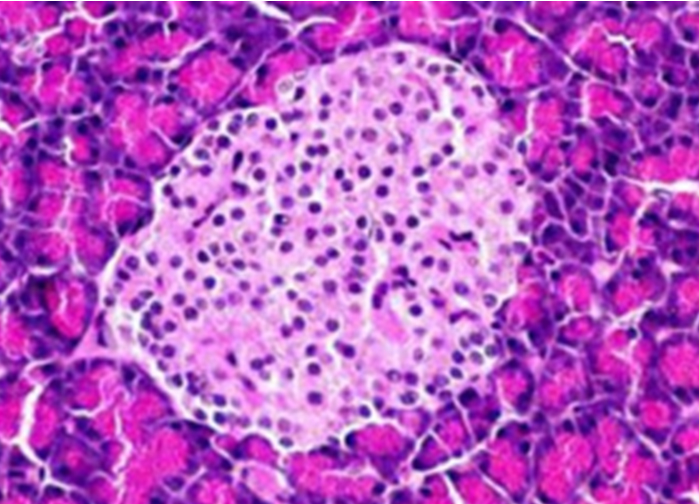
Рисунок 8. Поджелудочная железа (модель диабета, применение экстракта клюквы). Повреждение островка Лангерганса, некоторая деградация, но более сохраненная структура по сравнению с рис 2. Окраска гематоксилином и эозином. Увеличение × 200.
Зафиксированные нами эффекты в определенной степени укладываются в ранее описанный механизм антиоксидантного и противовоспалительного действия полифенолов — антоцианов темно-окрашенных ягод, включая клюкву, бруснику, чернику, голубику американского и европейского происхождения [19]. Расширенное (по спектру экстрактов — включение голубики и регионов происхождения — добавление Северо-Западной Сибири) описание эффектов полифенольных экстрактов ягод на модели сахарного диабета II типа может найти общие закономерности и создать основу для будущих клинических исследований. Перспективность такого подхода определяется тем обстоятельством, что сахарный диабет стал одной из основных проблем здравоохранения, а неадекватное регулирование уровня сахара в крови влечет за собой серьезные последствия для здоровья. Мы согласны с утверждением исследователей из 28 универсистетских центров Европы, Америки и Азии [20], заявляющих о том, что полифенольные экстракты растений, включая северные ягоды, содержашие полифенолы – антоцианы, могут в перспективе выступать в качестве альтернативного источника противодиабетических эффектов.
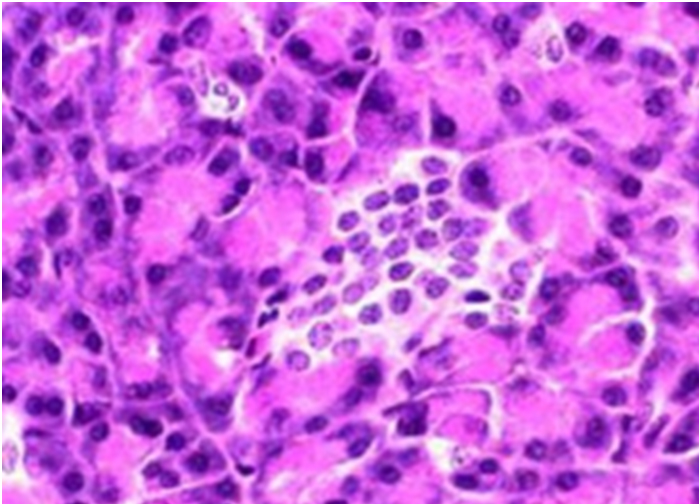
Рисунок 9. Поджелудочная железа (модель диабета, применение экстракта брусники). Повреждение островка Лангерганса, деградация структуры, репаративные процессы выражены слабо, картина сходная с рис 2. Окраска гематоксилином и эозином. Увеличение × 200.
ЛИТЕРАТУРА
1. Zuo L., Prather E.R., Stetskiv M., et al. Inflammaging and Oxidative Stress in Human Diseases. From Molecular Mechanisms to Novel Treatments. Int J Mol Sci. 2019, Sep. 10. Vol.20(18). PII: E4472. DOI: 10.3390/ijms20184472.
2. Jaganjac M., Milkovic L., Gegotek A., Cindric M, Zarkovic K., Skrzydlewska E., Zarkovic N. The relevance of pathophysiological alterations in redox signaling of 4-hydroxynonenal for pharmacological therapies of major stress-associated diseases. Free Radic Biol Med. 2019, Nov. 19. PII: S0891-5849(19)31639-9.
3. Moldogazieva N.T., Mokhosoev I.M., Mel’nikova T.I., Porozov Y.B., Terentiev A.A. Oxidative Stress and Advanced Lipoxidation and Glycation End Products (ALEs and AGEs) in Aging and Age-Related Diseases. Oxid Med Cell Longev. 2019, Aug. 14. 3085756. DOI: 10.1155/2019/3085756.
4. Gheibi S., Kashfi K., Ghasemi A. A. Practical guide for induction of type-2 diabetes in rat: Incorporating a high-fat diet and streptozotocin; Biomed Pharmacother; 2017, Nov; 95: 605-613.
5. Mazo V.K., Sidorova Y.S., Zorin S.N., Kochetkova A.A. Streptozotocin induced diabetes rat models; Vopr Pitan; 2016; 85(4):14-21.
6. Stull A.J. Blueberries’ Impact on Insulin Resistance and Glucose Intolerance; Antioxidants (Basel); 2016, Nov. 29; 5(4). PII: E44.
7. Roopchand D.E., Kuhn P., Rojo L.E., Lila M.A., Raskin I. Blueberry polyphenol-enriched soybean flour reduces hyperglycemia, body weight gain and serum cholesterol in mice; Pharmacol Res; 2013, Feb; 68(1):59-67.
8. Kleinert M., Clemmensen C., Hofmann S.M., et al. Animal models of obesity and diabetes mellitus; Nat Rev Endocrinol; 2018, Mar;14(3):140-162.
9. Bonora E., Moghetti Р., Zancanaro С., et al. Estimates of in vivo insulin action in man: Comparison of insulin tolerance tests with euglycemic and hyperglycemic glucose clamp studies; J. Clin. Endocrinol. Metab; 1989; 68:374–378.
10. Livak K.J., Schmittgen T.D. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T)) Method; Methods; 2001, Dec; 25(4):402-8.
11. Ito F., Ito H., Suzuki Ch., Yahata T., Ikeda K., Hamaoka K. The Application of a Modified d-ROMs Test for Measurement of Oxidative Stress and Oxidized High-Density Lipoprotein; Int J Mol Sci; 2017, Feb;18(2):454-462.
12. Różańska D., Regulska-Ilow B. Anthocyanins in prevention of type 2 diabetes. Adv Clin Exp Med. 2018; 27(1):135–142.
13. Lutz T.A. Considering our methods: Methodological issues with rodent models of appetite and obesity research; Physiol Behav; 2018, Aug; 1;192:182-187.
14. Ayoub H.M., McDonald M.R., Sullivan J.A., et al. The Effect of Anthocyanin-Rich Purple Vegetable Diets on Metabolic Syndrome in Obese Zucker Rats; J Med Food; 2017, Dec; 20(12):1240-1249.
15. Scazzocchio B., Varì R., Filesi C., et al. Cyanidin-3-O-b-glucoside and protocatechuic acid exert insulin-like effects by upregulating PPARγ activity in human omental adipocytes; Diabetes; 2011; 60:2234–2244.
16. Nemes A., Homoki J.R., Kiss R., et al. Effect of Anthocyanin-Rich Tart Cherry Extract on Inflammatory Mediators and Adipokines Involved in Type 2 Diabetes in a High Fat Diet Induced Obesity Mouse Model. Nutrients. 2019, Aug.21; Vol.11(9). PII: E1966. DOI: 10.3390/nu11091966.
17. Skrovankova S., Sumczynski D., Mlcek J., Jurikova T., Sochor J. Bioactive Compounds and Antioxidant Activity in Different Types of Berries; Int J Mol Sci; 2015, Oct.16; 16(10):24673-706.
18. Diaconeasa Z., Iuhas C.I., Ayvaz H., et al. Phytochemical Characterization of Commercial Processed Blueberry, Blackberry, Blackcurrant, Cranberry, and Raspberry and Their Antioxidant Activity. Antioxidants (Basel). 2019, Nov.10. Vol. 8(11). PII: E540. DOI: 10.3390/antiox8110540.
19. Kalt W., Cassidy A., Howard L.R., Krikorian R., Stull A.J., Tremblay F., Zamora-Ros R.Recent Research on the Health Benefits of Blueberries and Their Anthocyanins; Adv Nutr; 2019, Jul.22; PII: nmz065.
20. Salehi B., Ata A., Anil Kumar N., et al. Antidiabetic Potential of Medicinal Plants and Their Active Components; Biomolecules. 2019, Sep.30. Vol. 9(10). PII: E551. DOI: 10.3390/biom9100551.
Авторы
Кривых Елена Алексеевна
Бюджетное учреждение высшего образования Ханты-Мансийского автономного округа – Югры «Ханты-Мансийская государственная медицинская академия»
Кандидат медицинских наук, доцент, заведующая кафедрой общественного здоровья и здравоохранения
Российская Федерация, 628011, Тюменская область, Ханты-Мансийский автономный округ – Югра, г. Ханты-Мансийск, ул. Мира, д.40
KrivyhEA@hmgma.ru
Гуляев Александр Евгеньевич
Частное учреждение «National Laboratory Astana» Назарбаев университет
Доктор медицинских наук, профессор, научный консультант РГП «Национальный центр биотехнологии»
Республика Казахстан, 010000, г. Нур-Султан, Кабанбай-батыра, д. 53
akin@mail.ru
Коваленко Людмила Васильевна
Бюджетное учреждение высшего образования Ханты-Мансийского автономного округа – Югры «Сургутский государственный университет»
Доктор медицинских наук, профессор, заведующая кафедрой патофизиологии и общей патологии, директор медицинского института
Российская Федерация, 628412, Тюменская область, Ханты-Мансийский автономный округ – Югра, г. Сургут, ул. Энергетиков, д. 22
medsurdirector@gmail.com
Шульгау Зарина Токтамысовна
«Национальный центр биотехнологии» Республики Казахстан
Кандидат медицинских наук, заведующая лабораторией токсикологии и фармакологии
Республика Казахстан, 010000, г. Нур-Султан, Кургальжинское шоссе, здание 13/5
shulgau@biocenter.kz

