Анализ прогностической значимости экспрессии эктонуклеотизады CD39 периферическими Treg-клетками у больных колоректальным раком
УДК 616-006.6:571.27
Г.А. Жулай¹, Е.К. Олейник¹, М.И. Шибаев²,
П.Н. Семакова¹, В.М. Олейник¹
¹ФГБУН Федеральный исследовательский центр «Карельский научный центр Российской академии наук», г. Петрозаводск, Российская Федерация;
²ГБУЗ «Республиканский онкологический диспансер», г. Петрозаводск, Российская Федерация
Резюме. Регуляторные Т-лимфоциты (Treg) рассматриваются как потенциальные мишени при иммунотерапии рака и как прогностические биомаркеры течения заболевания. При некоторых типах рака, в том числе колоректального (КРР), роль Treg-клеток четко не определена и требует дальнейших исследований. В последнее время особое внимание уделяется способности Tregs экспрессировать эктонуклеотидазу CD39 в связи с ее участием в расщеплении аденозинтрифосфата до внеклеточного аденозина, который ингибирует противоопухолевый иммунный ответ. Повышенное содержание CD39⁺ Treg клеток отмечается как в опухолевой ткани, так и в периферической крови онкологических больных. Поэтому основной целью настоящего исследования было оценить прогностическую значимость уровня экспрессии (низкая/высокая) Treg-клетками эктонуклеотидазы CD39 в периферической крови у больных КРР. Материал и методы. В работе анализировали лимфоциты крови 32 больных КРР, группу сравнения составили 30 здоровых доноров. Относительное содержание Treg-клеток оценивали методом многоцветной проточной цитометрии на приборе Cytomics FC500 (Beckman Coulter, США) с использованием моноклональных антител CD4-FITC, CD25-PC5, CD127-PC7, CD39-PE. Экспрессию мРНК гена CD39 определяли методом полимеразной цепной реакции в реальном времени. Построение кривых выживаемости проводили при помощи процедуры Каплана–Мейера с применением логрангового критерия. Результаты. Ранее нами было установлено, что у больных КРР повышено содержание CD39⁺ Treg-клеток как в периферической крови по сравнению со здоровыми донорами, так и среди опухоль-инфильтрирующих клеток. Причем доля CD39-позитивных Treg-клеток увеличивалась по мере развития заболевания. В данной работе была проанализирована трехлетняя общая выживаемость больных КРР с учетом содержания CD39⁺ Treg-клеток (CD4⁺CD25⁺CD127lo/-) и в зависимости от уровня мРНК гена CD39 в периферической крови. Не выявлено статистически значимых различий по выживаемости больных в зависимости от содержания CD39⁺ Treg-клеток и уровня мРНК гена CD39. Заключение. Дальнейшее изучение аденозинового механизма иммунной супрессии с участием регуляторных клеток Tregs позволит открыть новые терапевтические и прогностические возможности при ведении больных КРР, что представляет большой научный и практический интерес.
Ключевые слова: колоректальный рак, регуляторные Т-клетки, эктонуклеотидаза, CD39, общая выживаемость
Конфликт интересов отсутствует.
Контактная информация автора, ответственного за переписку:
Жулай Галина Анатольевна
zhgali-111@yandex.ru
Дата поступления 16.11.2020 г.
Образец цитирования:
Жулай Г.А., Олейник Е.К., Шибаев М.И., Семакова П.Н., Олейник В.М. Анализ прогностической значимости экспрессии эктонуклеотизады CD39 периферическими Treg-клетками у больных колоректальным раком. http://vestnikural.ru/article/1154 [Электронный ресурс] Вестник уральской медицинской академической науки. 2020, Том 17, №4, с. 323–332, DOI: 10.22138/2500-0918-2020-17-4-323-332
Введение
Колоректальный рак (КРР) является одной из ведущих локализаций среди злокачественных новообразований в общей структуре онкологической заболеваемости в России и в мире [1]. Своевременное выявление этого заболевания, а также идентификация молекулярных мишеней, позволяющих прогнозировать течение заболевания и эффективность терапии, является в настоящее время одной из актуальных медико-социальных задач.
Растущая опухоль использует различные механизмы для уклонения от иммунологического надзора. Одним из таких способов является индукция иммунной супрессии для подавления противоопухолевого иммунного ответа. Непосредственными участниками этого процесса являются регуляторные Т-клетки (Treg). Эти клетки в норме подавляют чрезмерный иммунный ответ в организме, поддерживая иммунологическую толерантность и препятствуя развитию аутоиммунных реакций. В некоторых случаях супрессорные Treg-клетки могут способствовать развитию опухоли. Treg-клетки присутствуют в высоком количестве в периферической крови и опухолевой ткани различных типов и локализаций рака. Повышенное содержание CD4⁺ Treg-клеток среди опухоль-инфильтрирующих лимфоцитов часто сопровождается снижением соотношения CD8+ Т-клеток и CD4⁺CD25⁺FOXP3⁺ Treg-клеток и ассоциируется с неблагоприятным прогнозом для большинства больных со злокачественными новообразованиями [2]. Отмечается, что Treg-клетки могут препятствовать успешной противоопухолевой терапии. В связи с этим детальное исследование взаимосвязи иммунных клеток и опухоли при КРР позволит выявить иммунологические мишени, которые могут быть использованы в клинике.
CD39 или эктонуклеозид трифосфат дифосфогидролаза-1, мембранный белок, который связывает внеклеточный аденозин трифосфат и преобразует его с участием CD73 во внеклеточный аденозин, обладающий иммуносупрессорным эффектом и способствующий канцерогенезу [3, 4]. CD39 экспрессируется различными иммунными и не иммунными клетками (эндотелиальные, фибробласты), а также некоторыми опухолевыми клетками. Отмечается, что опухоль-инфильтрирующие иммунные клетки демонстрируют усиленную экспрессию CD39. В настоящее время блокада аденозинового механизма супрессии рассматривается как потенциальное направление иммунотерапии онкологических больных.
Установлено, что Treg-клетки могут участвовать в образовании аденозина из внеклеточных нуклеотидов, что рассматривается как один из основных механизмов их супрессорной активности [5]. В условиях развития рака Treg-клетки отличаются повышенной экспрессией CD39 как в микроокружении опухоли, так и на периферии [6]. Ранее нами была показана активация аденозин-опосредованной супрессии у больных КРР [7], при которой немаловажную роль может играть популяция CD39⁺ Treg-клеток. В связи с этим целью данной работы было оценить прогностическую значимость уровня экспрессии (низкая/высокая) Treg-клетками эктонуклеотидазы CD39 в периферической крови у больных КРР.
Материалы и методы
В работе обследованы 32 пациента с КРР, средний возраст которых составил 64±11,5 лет. В исследование включались больные, соответствующие критериям: возраст 18–70 лет, наличие подтвержденного диагноза «колоректальный рак». Диагноз КРР устанавливался на основании клинических, лабораторных, эндоскопических и морфологических методов исследования. Критериями исключения являлись: наличие других форм новообразований в анамнезе, а также иммуновоспалительных заболеваний. Пациенты были разделены на две группы: в первую группу входили больные на I и II стадиях КРР (n=17), во вторую — на III и IV стадиях (n=15). Для проведения исследования было получено разрешение Комитета по медицинской этике при Министерстве здравоохранения и социального развития Республики Карелия и Петрозаводском государственном университете (протокол №25 от 12.02.2013 г.). От обследованных больных получено информированное согласие на исследование. В качестве группы сравнения анализировали лимфоциты 30 здоровых доноров в возрасте 54,4±20,6 лет.
В работе проводили исследование иммунофенотипа лимфоцитов больных КРР методом многоцветной проточной цитометрии на приборе Cytomics FC500 (Beckman Coulter, США). Использовались моноклональные антитела CD4-FITC, CD25-PC5, CD127-PC7 (Beckman Coulter, Франция), CD39-PE (R&DSystems, США) и соответствующие изотипические контроли. Экспрессию мРНК гена CD39 определяли методом ПЦР в реальном времени. Выделение и очистку нуклеиновых кислот проводили с помощью набора «AxyPrep Blood Total RNA Miniprep Kit» (Axygen, США). Для синтеза кДНК использовали случайные гексапраймеры и MMLV-обратную транскриптазу (Силекс, Россия). Амплификацию кДНК, а также анализ продуктов амплификации в режиме реального времени выполняли с использованием реакционной смеси с интеркалирующим красителем SYBR Green I (Евроген, Россия) на приборе «iCycler Thermal Cycler» (Bio-Rad, США). Анализ полученных данных проводили методом 2–∆∆Ct, где Сt — пороговый цикл, а ∆Сt — разница между значениями пороговых циклов для референсного (GAPDH) и таргетного генов. Итоговый уровень экспрессии исследуемого гена рассчитывали относительно контроля (здоровые доноры), принимая за единицу величину экспрессии исследуемого гена в контроле.
Статистическую обработку результатов, полученных в ходе исследования, проводили с использованием программ GRAPH Pad Prism 6.0. Построение кривых выживаемости проводили при помощи процедуры Каплана–Мейера. При сравнении кривых выживаемости в группах применяли логранговый критерий. Цензурированные данные включали данные больных, которые были живы на момент окончания исследования. Нецензурированные данные — данные умерших больных. Уровень статистической значимости был принят равным 0,05. Анализ выживаемости и визуализацию выполняли с помощью программы IBM SPSS Statistics Subscription. Исследование выполнено на научном оборудовании «Центра коллективного пользования Федерального исследовательского центра «Карельский научный центр Российской академии наук» (ЦКП КарНЦ РАН).
Результаты и обсуждение
Ранее нами было показано, что у больных КРР повышено содержание CD39⁺ Treg-клеток как в периферической крови по сравнению со здоровыми донорами, так и среди опухоль-инфильтрирующих клеток. Причем доля CD39-позитивных Treg-клеток увеличивалась по мере развития заболевания [7].
В данной работе была проанализирована трёхлетняя общая выживаемость (ОВ) 32 больных КРР с учетом содержания CD39⁺ Treg-клеток (CD4⁺CD25⁺CD127lo/-) в периферической крови. Больные были разделены на две группы в зависимости от значения M+2SD содержания (более или менее) CD39⁺ Treg-клеток у здоровых лиц, которое составило 65,36%. Отмечено, что ОВ в группе с низким содержанием CD39⁺ Treg-клеток равна 64,3% при средней выживаемости 26,3±3,5 месяца (95% ДИ 19,3-33,3 месяца) и не отличалась от группы с высоким содержанием CD39⁺ Treg-клеток, где составила 61,1% при средней выживаемости 25,9±3,7 месяцев (95% ДИ 18,5-33,3 месяца, p=0,79) (рисунок). Анализ выживаемости больных с учетом этого фактора не показал статистически значимых различий и при рассмотрении данных в зависимости от стадии заболевания (табл. 1).
Таблица 1
Трехлетняя общая выживаемость больных колоректальным раком в группах с низким и высоким содержанием CD39⁺ Treg-клеток в периферической крови
Table 1
Three-year overall survival of patients with colorectal cancer in groups with low and high frequency CD39⁺ Treg cells in peripheral blood
Группы / Groups | Общая выживаемость, все больные/ Overall survival, all patients | Общаявыживаемость, I-II стадии/ Overall survival, stages I-II | Общаявыживаемость, III-IV стадии/ Overall survival, stages III-IV |
Низкоесодержание CD39⁺ Treg-клеток/ Low frequency of CD39⁺ Treg cells | 64,3% | 88,9% | 20% |
Высокоесодержание CD39⁺ Treg-клеток / Hight frequency of CD39⁺ Treg cells | 61,1% | 87,5% | 44,4% |
Примечание. Treg-клетки определяли по фенотипу CD4⁺CD25⁺CD127lo/-
Note. Treg cells were determined as CD4⁺CD25⁺CD127lo/-
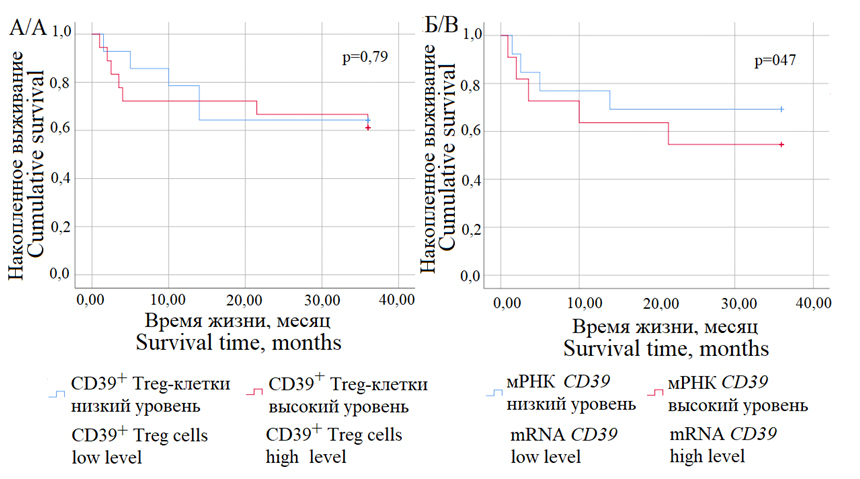
Рисунок. Кривые Каплана-Мейера. А. — Влияние на общую выживаемость изменения содержания CD39⁺ Treg-клеток (CD4⁺CD25⁺CD127lo/-) в периферической крови больных КРР. Б. — Влияние на общую выживаемость изменения медианы экспрессии мРНК CD39 в периферической крови больных КРР
Figure. Kaplan-Meier curves. A — overall survival and frequency of CD39⁺ Treg-cells (CD4⁺CD25⁺CD127lo/-) in the peripheral blood of patients with CRC. B — overall survival and level of mRNA CD39 in peripheral blood of CRC patients
В предыдущем исследовании [7] было также установлено, что больные КРР отличались повышенным уровнем экспрессии мРНК гена CD39 в лейкоцитах крови. В связи с этим в работе была проанализирована трехлетняя ОВ больных КРР в зависимости от уровня мРНК гена CD39. Высокий и низкий уровень экспрессии мРНК CD39 определяли по медиане. В группе больных с низким уровнем экспрессии мРНК CD39 ОВ составила 69,2% при средней выживаемости 14,1±6,7 месяцев (95% ДИ 1,0-27,3) против ОВ в 54,5% при средней выживаемости 16,7±6,2 месяцев (95% ДИ 4,4-30,0) в группе с высоким уровнем экспрессии мРНК этой эктонуклеотидазы. Значимых различий между этими группами не выявлено, p=0,47 (рисунок, табл. 2), ОВ в группах с высокой и низкой экспрессией мРНК CD39 в зависимости от стадии заболевания также статистически не отличалась (табл. 2).
Таблица 2
Трехлетняя общая выживаемость больных колоректальным раком в группах с высоким и низким уровнем экспрессии мРНК CD39 в лейкоцитах периферической крови
Table 2
Three-year overall survival of patients with colorectal cancer in groups with high and low CD39 mRNA levels in peripheral blood leukocytes
Группы/ Groups | Общая выживаемость, все больные/ Overall survival, all patients | Общая выживаемость, I-II стадии/ Overall survival, stages I-II | Общая выживаемость, III-IV стадии/ Overall survival, stages III-IV |
Низкий уровень экспрессии мРНК CD39/ LowCD39 mRNAlevel | 69,2% | 90,0% | 25,0% |
Высокий уровень экспрессии мРНК CD39/ HighCD39 mRNAlevel | 54,5% | 75,0% | 33,3% |
В настоящее время показано, что при многих злокачественных заболеваниях накопление Treg-клеток в опухолевой ткани и последующее снижение соотношения CD8+-клеток к Treg-клеткам коррелирует с неблагоприятным прогнозом для больных [2]. Однако в отношении таких типов рака, как КРР и опухоли головы и шеи, существуют противоречивые сведения о прогностической роли Treg-клеток. Результаты некоторых исследований демонстрируют, что увеличение содержания Тreg-клеток ассоциировано с положительной динамикой заболевания. Предполагается, что на длительность выживаемости сказывается ограничение инфильтрирующими FOXP3⁺ Treg-клетками воспалительного ответа, вызванного кишечной микробиотой на ранних стадиях КРР [8].
Исследованиями последних лет было установлено, что в микроокружении опухоли активно накапливается внеклеточный аденозин, оказывающий иммуносупрессорное действие и способствующий канцерогенезу. Образование аденозина происходит благодаря слаженной работе эктонуклеотидаз CD39 и CD73, которые расщепляют высвобождаемый в условиях внутриопухолевой гипоксии аденозинтрифосфат. Высокая экспрессия генов СD39/CD73 и их продуктов показана многими опухолевыми клетками и клетками, находящимися в микроокружении опухоли, и имеет потенциальную значимость в качестве прогностического фактора. Примечательно, что прогностическая роль экспрессии в опухоли CD73 исследована лучше и рассматривается как неблагоприятный фактор при многих онкологических заболеваниях [9]. Значение экспрессии CD39 в опухолевой ткани исследовано меньше. Так, при злокачественных новообразованиях головы и шеи внутриопухолевая экспрессия молекулы CD39 была неблагоприятным фактором выживаемости больных [10], а при раке поджелудочной железы оказалась благоприятным фактором послеоперационной выживаемости [11]. Существует ряд исследований, посвященных определению роли CD39⁺ Treg-лимфоцитов в качестве потенциального маркера течения болезни и/или действия противоопухолевой терапии, чаще с применением блокаторов иммунных контрольных точек. Так, Cai с соавторами показали, что при гепатоцеллюлярной карциноме повышенное содержание CD39⁺FOXP3⁺-клеток было независимым неблагоприятным фактором ОВ больных после радикального удаления опухоли [12]. При меланоме накопление CD39⁺Treg-клеток в периферической крови также является неблагоприятным фактором ОВ и безрецидивной выживаемости [13, 14]. Отмечено, что при злокачественных новообразованиях головы и шеи увеличение количества CD39⁺Treg-клеток в крови ассоциировано с короткой ОВ больных, получающих ниволумаб [15].
Повышенная экспрессия эктонуклеотидазы CD39 продемонстрирована и при КРР как опухолевыми клетками, так и клетками крови на периферии [16, 17]. На мышиных моделях показано, что CD39 стимулирует рост и метастазы рака толстой кишки. Кроме того, результаты in vitro исследования показали, что применение ингибиторов активности CD39 или блокирующих антител ослабляло опухоль-индуцированную супрессию CD4⁺- и CD8+ Т-клеточной пролиферации и усиливало цитотоксическую активность ЦТЛ и NK-клеток [16]. Примечательно, что наряду с данными сведениями Zhang c соавт. показали, что экспрессия CD39 в эпителиальных клетках аденокарциномы прямой кишки человека коррелирует с благоприятным клиническим исходом болезни [17]. Несмотря на значимую усиленную экспрессию эктонуклеотидазы CD39 периферическими лимфоцитами, нами не было выявлено достоверной связи высокого/низкого уровня CD39⁺ Treg-клеток с выживаемостью обследованных больных. Также малоинформативным в этом отношении оказался уровень экспрессии мРНК гена CD39. По-видимому необходимо дальнейшее изучение аденозин-опосредованной иммунной супрессии, активация которой происходит у больных КРР, с целью определения особенностей функционирования клеток как внутри опухоли, так и среди циркулирующих лимфоцитов для разработки и повышения эффективности подходов в противоопухолевой иммунотерапии.
Заключение
В настоящее время подтверждена двоякая роль опухоль-инфильтрирующих лимфоцитов в микроокружении опухоли. Одни клетки способны распознавать и элиминировать неопластические клетки в ходе противоопухолевого иммунного ответа, другие, напротив, способствуют росту и метастазированию опухоли, создавая условия для уклонения трансформированных клеток от иммунного надзора. Меняющийся при этом молекулярный профиль иммуноцитов является перспективным в использовании клеточной терапии и поиске биомаркеров прогноза течения болезни и/или ее лечения. В настоящее время прогностическое значение Treg-клеток при развитии рака остается спорным для некоторых типов злокачественных новообразований, в частности, при колоректальном раке. Поэтому необходимы дальнейшие исследования для выявления предиктивной значимости иммунокомпетентных клеток при развитии рака и разработки эффективных способов их использования.
ЛИТЕРАТУРА
- Федоров В.Э., Поделякин К.А. Эпидемиологические аспекты колоректального рака. Медицинский альманах. 2017; 4(49): 145-148
- Tanaka, A. Sakaguchi, S. Targeting Treg cells in cancer immunotherapy. Eur. J. Immunol. 2019; 49: 1140-1146.
- Moesta, A.K., Li, X., Smyth, M.J. Targeting CD39 in cancer. Nat Rev Immunol. 2020.
- Головкин А.С., Асадуллина И.А., Кудрявцев И.В. Пуринергическая регуляция основных физиологических и патологических процессов. Медицинская иммунология. 2018; 20 (4): 463-476.
- Deaglio S., Dwyer K.M., Gao W., et al. Adenosine generation catalyzed by CD39 and CD73 expressed on regulatory T cells mediates immune suppression. J Exp Med. 2007; 204(6): 1257-1265.
- Schuler P.J., Schilling B., Harasymczuk M. et al. Phenotypic and functional characteristics of CD4⁺CD39⁺ FOXP3⁺ and CD4⁺CD39⁺FOXP3neg T‐cell subsets in cancer patients. Eur. J. Immunol. 2012; 42: 1876-1885.
- Жулай Г.А., Чуров А.В., Олейник Е.К. и др. Активация CD4⁺CD39⁺ Т-клеток при колоректальном раке. Вестник Российского государственного медицинского университета. 2018; 3: 49-55
- Saleh R., Elkord E. FOXP3⁺ T regulatory cells in cancer: Prognostic biomarkers and therapeutic targets. Cancer Lett. 2020; 490:174-185.
- Wang R., Zhang Y., Lin X., Gao Y., Zhu Y. Prognostic value of CD73-adenosinergic pathway in solid tumor: A meta-analysis and systematic review. Oncotarget. 2017; 8(34):57327-57336.
- Mandapathil M., Boduc M., Roessler M. et al. Ectonucleotidase CD39 expression in regional metastases in head and neck cancer. Acta Oto-Laryngologica. 2018; 138 (4): 428-432
- Künzli B.M., Berberat P.O., Giese T., et al. Upregulation of CD39/NTPDases and P2 receptors in human pancreatic disease. Am J Physiol Gastrointest Liver Physiol. 2007; 292 (1): G223-G230.
- Cai X.Y., Ni X.C., Yi Y. et al. Overexpression of CD39 in hepatocellular carcinoma is an independent indicator of poor outcome after radical resection. Medicine (Baltimore). 2016; 95(40): e4989.
- Retseck J., Nasr A., Lin Y. et al. Long term impact of CTLA4 blockade immunotherapy on regulatory and effector immune responses in patients with melanoma. J Transl Med. 2018; 16 (1): 184.
- Shevchenko A., Mathes C., Groth et al. Enhanced expression of CD39 and CD73 on T cells in the regulation of anti-tumor immune responses OncoImmunology. 2020; 9 (1): 1744946
- Ottonello S., Genova C., Cossu I., et al. Association between response to nivolumab treatment and peripheral blood lymphocyte subsets in patients with non-small cell lung cancer. Front Immunol. 2020; 7 (11):125.
- Hajizadeh F., Masjedi A., Heydarzedeh Asl. S. et al. Adenosine and adenosine receptors in colorectal cancer. Int Immunopharmacol. 2020; 87:106853.
- Zhang B., Cheng B., Li F.S. et al. High expression of CD39/ENTPD1 in malignant epithelial cells of human rectal adenocarcinoma. Tumour Biol. 2015; 36(12): 9411-9.
Финансовое обеспечение исследований осуществлялось из средств федерального бюджета на выполнение государственного задания КарНЦ РАН, бюджетная тема № 0218-2019-0083.
Авторы
Жулай Галина Анатольевна
Институт биологии — обособленное подразделение Федерального государственного бюджетного учреждения науки Федерального исследовательского центра «Карельский научный центр Российской академии наук» (ИБ КарНЦ РАН)
Младший научный сотрудник группы иммунологии
Российская Федерация, 185014, Республика Карелия, г. Петрозаводск, ул. Пушкинская, 11
zhgali-111@yandex.ru
Олейник Евгения Константиновна
Институт биологии — обособленное подразделение Федерального государственного бюджетного учреждения науки Федерального исследовательского центра «Карельский научный центр Российской академии наук» (ИБ КарНЦ РАН)
Доктор биологических наук, доцент, главный научный сотрудник, руководитель группы иммунологии
Российская Федерация, 185014, Республика Карелия, г. Петрозаводск, ул. Пушкинская, 11
ole@krc.karelia.ru
Шибаев Михаил Игоревич
Государственное бюджетное учреждение здравоохранения Республики Карелия «Республиканский онкологический диспансер»
Кандидат медицинских наук, эндоскопист, онколог, хирург
Российская Федерация, 185002, Республика Карелия, г. Петрозаводск, Лососинское шоссе,5
mshib@karelia.ru
Семакова Полина Николаевна
Институт биологии — обособленное подразделение Федерального государственного бюджетного учреждения науки Федерального исследовательского центра «Карельский научный центр Российской академии наук» (ИБ КарНЦ РАН)
Младший научный сотрудник группы иммунологии
Российская Федерация, 185014, Республика Карелия, г. Петрозаводск, ул. Пушкинская, 11
k-polina13@mail.ru
Олейник Виктор Михайлович
Институт биологии — обособленное подразделение Федерального государственного бюджетного учреждения науки Федерального исследовательского центра «Карельский научный центр Российской академии наук» (ИБ КарНЦ РАН)
Доктор биологических наук, ведущий научный сотрудник группы иммунологии
Российская Федерация, 185014, Республика Карелия, г. Петрозаводск, ул. Пушкинская, 11
scigraph@yandex.ru

