Экспериментальное обоснование иммуноцитотерапии нарушений кроветворения
В.В. Базарный, А.П. Ястребов, В.Н. Мещанинов
УДК 616.41:576.8.097.3
ГУЗ «Институт клеточных медицинских технологий»,
Уральская государственная медицинская академия, г. Екатеринбург
Иммуноцитотерапия – лечебное использование иммунокомпетентных клеток (ИКК) – относится к наиболее «наукоемким» лечебным технологиям, начало которой положили пересадки костного мозга. В настоящее время она включает широкий круг вопросов, связанных с созданием вакцин (например основанных на использовании дендритных клеток), адоптивной иммунотерапией (лечебное применение эффекторных клеток, в частности LAK-, CIК-, TIL-терапия) и других. Одним из ее направлений является воздействие на репаративный потенциал ткани. Это стало возможным благодаря открытой у ИКК, прежде всего – лимфоцитов, морфогенетической функции [1]. Она заключается в способности лимфоидных клеток транспортировать регенераторную информацию в условиях адоптивного переноса. Перспективы лечебного использования данного феномена требуют уточнения, что и определило цель нашей работы – оценить эффективность трансплантации лимфоцитов различного происхождения на состояние костно-мозгового кроветворения на примере экспериментальной железодефицитной анемии (ЖДА).
Материалы и методы исследования
Эксперимент выполнен на 48 крысах-самцах породы Вистар. ЖДА моделировали путем повторных кровопусканий, введения железосвязывающего комплексона десферал и содержанием животных на обедненной железом диете. У животных определяли стандартные показатели кроветворения: число миелокариоцитов, миелограмма, общеклинический анализ крови с подсчетом ретикулоцитов, а также уровень сывороточного железа и общей железосвязывающей способности сыворотки (ОЖСС) бетафенантроллиновым способом с использованием тестсистем «Лахема» [2]. Для оценки синтетических процессов оценивали включение меченого 3Н-тимидина в миелокариоциты [3]. Результаты выражали в беккерелях на 1 млн клеток. Данный фрагмент исследования выполнен совместно с проф. О.Г. Макеевым.
После развития у крыс ЖДА им с целью коррекции вводили лимфоциты доноров следующих групп:
1) интактные тимоциты,
2) тимоциты, полученные от животных, подвергнутых гипоксическому воздействию в течение шести часов в барокамере приточно-вытяжного типа с разряжением воздуха до 40 КПа, что индуцирует появление у клеток «эритропоэзстимулирующих» свойств [4],
3) смесь из равных частей тимоцитов и спленоцитов от животных, полученным аналогичным способом,
4) тимоциты интактых животных, преинкубированнные в течение двух часов перед трансплантацией в культуральной среде, содержащей неспецифический митоген – ФГА.
Трансплантацию донорских клеток реципиентов осуществляли в асептических условиях в каудальную вену в количестве 100х106 лимфоцитов на 100 г массы животного. Влияние трансплантации на кроветворение оценивали через 72 часа.
Статистическую обработку результатов осуществляли стандартными способами вариационной статистики.
Результаты и их обсуждение
Трансплантация интактных тимоцитов, как было показано нами в предварительных экспериментах и частично – в данном исследовании, не вызвала существенных изменений кроветворения у нормальных и «железодефицитных» реципиентов. Под влиянием «гипоксических» тимоцитов отчетливо видны признаки стимуляции эритропоэза. Это проявляется увеличением числа эритроидных клеток в костном мозге, что сопровождается усилением в нем синтетических процессов (табл. 1).
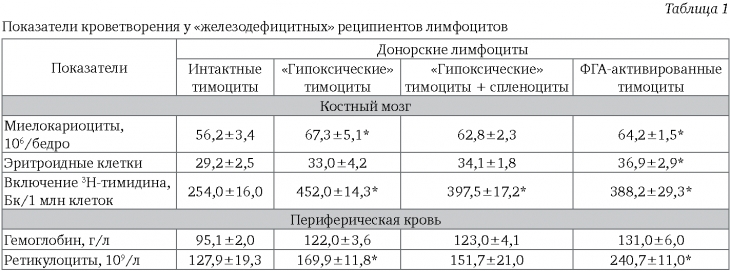
Одновременно увеличилась концентрация гемоглобина и содержание ретикулоцитов в периферической крови. Внесение в «трансплантат» селезеночных клеток существенно не изменило эритропоэтический эффект, а степень ответа у реципиентов была даже несколько ниже. Это указывает скорее всего на то, что преимущественную роль в стимуляции эритропоэза играют молодые Т-лимфоциты, которые составляют основную часть клеток, полученных из тимуса. Взвесь спленоцитов крысы состоит примерно из равных частей Т- и В-клеток. Вероятно, В-лимфоцитам не присуща подобная эритропоэзстимулирующая активность, чем и обусловлен результат трансплантации.
Обработка тимоцитов ФГА также вызывала у них появление эритропоэтических свойств. В частности, число ретикулоцитов в крови увеличилось практически в два раза в сравнении с контролем. Возможно, это связано с тем обстоятельством, что подвлиянием данного митогена усиливается продукция
цитокинов иммунокомпетентными клетками, в том числе – и обладающих бурстпромоторной активностью.
Следует отметить, что под влиянием трансплантации ИКК существенно не изменились показатели обмена железа у крыс с ЖДА. Вероятно, это можно объяснить усилением утилизации депонированного железа, обеспечивающего гемоглобинизацию эритроцитов.
Таким образом, у «железодефицитных» реципиентов после трансплантации «гипоксических» или ФГА-активированных лимфоцитов нормальных доноров через 72 часа после трансплантации клеток отмечается стимуляция эритропоэза. Последнее связано с миграцией трансплантируемых лимфоцитов в костный мозг, где происходит их межклеточная кооперация с кроветворными предшественниками при участии цитокинов [5, 6].
Следовательно, трансплантация активированных лимфоцитов оказывает влияние на функциональную активность костного мозга, в значительной степени – через взаимодействие со стволовыми кроветворными клетками, что может рассматриваться как один из потенциальных способов ее регуляции.
ЛИТЕРАТУРА
1. Бабаева А.Г. Регенерация и система иммуногенеза [Текст]/А.Г. Бабаева. – М.: Медицина, 1985. – 256 с.
2.Клиническая лабораторная аналитика. Том 2. [Текст]: справочник //Под ред. В.В. Меньшикова. – М.: Лабинформ-РАМЛД. – 1999. – 352 с.
3. Макеев О.Г. Применение радионуклидов для характеристики регенерации тканей при повреждении [Текст] / О.Г. Макеев//Применение радионуклидов и ионизирующих излучений в народном хозяйстве и научных исследованиях: Сб. научн. тр. – Свердловск, 1983. – С. 59 – 60.
4. Об участии клеточных систем иммунитета в регенерации при экстеремальных воздействиях [Текст]/ М.В. Попугайло, А.М. Наливайко, Е.С. Тихачек, В.В. Базарный// Механизмы аварийного регулирования и адаптации при действии на организм экстремальных факторов. Сб. научн. трудов. – Свердовск: СГМИ, 1984. – С. 20 – 25.
5. Regulation of hematopoiesis in vitro and in vivo by invariant NKT cells [Text]/ I. Kotsianidis, J.D. Silk, E. Spanoudakis, S. Patterson et al.// Blood. – 2006. – Vol. 107. – P. 3138 – 3144.
6. Prospective isolation and global gene expression analysis of the erythrocyte colony-forming unit (CFU-E) [Text]/G. Terszowski, C. Waskow, P.Conradt, D. Lenze et al.//Blood. – 2005, Vol. 105. – P.1937 – 1945.

